Canlıların Yapısında Bulunan Temel Bileşikler Hangileridir? Organik Bileşikler, Canlılığa Nasıl Hayat Verir?
Hayat Moleküllerinin Temelleri, Oluşumları, Görevleri ve Canlılık Konusundaki Etkileri Nelerdir?
/old/content_media/2639ae22922475c429b9e0da4228249d.jpg)
- Özgün
- Moleküler Evrim
- Abiyogenez
Yazı dizisi içindeki ilerleyişinizi kaydetmek için giriş yapın veya kayıt olun.
Bu Makalede Neler Öğreneceksiniz?
- Hayat molekülleri karbon, hidrojen, oksijen, azot, fosfor ve sülfür atomlarından oluşan nükleotitler, lipitler, proteinler ve karbonhidratlardır ve canlılığın temel yapı taşlarıdır.
- Karbonun dört kovalent bağ yapabilme özelliği ve karbon-karbon bağlarının çeşitliliği, milyonlarca farklı molekülün oluşmasını sağlayarak canlılığın kimyasal çeşitliliğini mümkün kılar.
- Proteinler aminoasitlerin peptit bağlarıyla birleşmesiyle oluşur, yapıları işlevlerini belirler ve enzimler gibi kimyasal tepkimeleri hızlandırarak canlı organizmaların hayatta kalmasını sağlar.
Hayat Molekülleri, ya da diğer bir ismiyle organik moleküller en azından bizim bildiğimiz ve tanımladığımız anlamıyla canlılığın var olabilmesi ve varlığını sürdürebilmesi için gereken kimyasal moleküllerdir. Temel olarak nükleotitler, lipitler, proteinler ve karbonhidratlar "hayat molekülleri"dir. Bu moleküllerin hepsinin genel formları az çok benzer olsa da, işlevleri kimyasal ve fiziksel özelliklerinden dolayı birbirlerinden tamamen farklıdır.
Bu farklı özelliklerin toplamı, bugün bizlerin "canlı" olarak isimlendirdiği varlık formlarını meydana getirir. Daha doğrusu, canlılık için gereken aktivite ve organizasyon şartlarının istikrarlı bir şekilde sağlanabilmesi için bu kimyasallardan oluşan bir yapı ve bu yapının uzun süreli deneme-yanılma ve eleme-seçme mekanizmalarından geçmesi gerekmektedir. Dolayısıyla, şimdilik bildiğimiz kadarıyla, bu moleküllerden oluşmayan bir varlığın canlılığın ilkelerini bir arada bulundurması pek mümkün değildir. Bunda, bu moleküllerin istikrarlı yapısının (tepkimeler, radyoaktivite, vb. kimyasal özellikler bakımından) çok büyük önemi olduğunu unutmamak gerekmektedir.
Hayat Moleküllerine Daha Yakından Bir Bakış...
Burada akla şu soru gelebilir: "Organik moleküller" tam olarak hangi atomlardan oluşur? Yani bu tür molekülleri barındıran yapıları "canlı" kılan elementler hangileridir? Cevap açıktır: Karbon (C), Hidrojen (H), Oksijen (O), Nitrojen (N), Fosfor (P) ve Sülfür (S). Yani bir canlıya "canlılık" özelliğini katan molekülleri oluşturan atomlar, tam da bekleneceği gibi, periyodik cetvel üzerinde bulunan sıradan atomlardır ve tek başlarına herhangi bir özel durumları bulunmamaktadır. Bu da bize, bir kez daha, canlılığın cansızlıktan yapısal olarak bir farkı olmadığını yeniden göstermektedir. Elimizdeki "canlılık problemi", bir elementer organizasyon (moleküler düzenlenme hiyerarşisi) problemidir; özünde bu iki yapı arasında temel bir fark yoktur.
Karbon Kimyası Neden İlginç ve Önemlidir?
Burada karbonun özel bir yeri vardır ve bunun, temelde 2 nedeni vardır: Öncelikle karbon atomlarının etrafında dönen ve "boşta" olan 4 elektronları vardır. Bu elektronlar sayesinde karbon atomları, diğer elementlerle 4 kovalent bağ kurabilir. Karbonun bağlanabildiği element çeşitliliği de oldukça yüksektir: hidrojen, oksijen, fosfor, sülfür ve azot, bunlardan sadece birkaçıdır. Karbonun bu esnek ve çok yönlü yapısı, çok sayıda farklı karmaşık molekülü mümkün kılar ve bu karmaşık moleküller de bir araya gelerek canlılığı oluşturur.
Karbonu ilginç kılan ikinci neden, karbon atomlarının birbirleriyle bağ kurabiliyor olmasıdır. Karbon atomları birbirlerine bağlanarak çok daha uzun zincirler inşa edebilirler; öyle ki, teknik olarak bu zincirlerin uzunluğu konusunda bir sınır yoktur (mekanik limitler haricinde). Dahası, bu karbon-karbon bağları tekli bağlar, ikili bağlar veya üçlü bağlar şeklinde de olabilir; yani inşa edilen bağların gücü de duruma ve komşu atomlara bağlı olarak değişebilir. Bu da, karbon kimyasına çok geniş bir çeşitlilik katmaktadır: Karbon atomları üzerine, milyonlarca farklı molekül inşa etmek mümkündür! Periyodik cetveldeki diğer hiçbir element, karbondaki bu çeşitliliğe sahip değildir ve bu nedenle, canlılığın temelinde de karbon atomlarını bulmamız şaşırtıcı değildir. Yaşam, onu istatistiki olarak mümkün kılma olasılığı en yüksek element etrafında oluşmuştur.
Şekerler (Karbonhidratlar): Yapıları, Özellikleri ve Oluşumları
Karbonhidrat, "hidratlanmış karbon" anlamına gelmektedir ve "hidro-" kökü, bir molekülün su (H2O) ile ilişkili olduğunu bildirmektedir. Yani bu moleküller içerisinde karbon, hidrojen ve oksijen bir arada bulunur. Hatta sadece bir arada bulunmakla kalmaz, su içerisinde bulunduklarıyla aynı oranda, yani 2'ye 1 (2:1) oranında bulunurlar. Bir diğer deyişle, karbonhidratların moleküler formülü (CH2O)n olarak verilir; çünkü her zaman 1 karbon, 2 hidrojen, 1 oksijen atomu ve bunların katları şeklinde inşa edilirler.
Karbonhidratlara "şeker" denmesinin nedeni, diğer isimlerinin "sakkarit" olmasıdır (bu kelime, "şeker" anlamına gelmektedir). Şekerler; özellikle de glikoz (İng: "glucose") ve fruktoz (İng: "fructose" veya daha yaygın ismiyle "meyve şekeri") gibi basit şekerler, canlılar için hayati öneme sahiptir. Bu basit şekerler, aynı zamanda monosakkarit ("basit şeker" veya "tek şeker") olarak da bilinir ve canlıların yapısında bulunabilen birçok kompleks şeker molekülünün (nişasta, glukojen, kitin, selüloz, vb.) temelini oluştururlar. Aşağıda, canlılarda en çok kullanılan bazı karbonhidratların (şekerlerin) kimyasal yapılarını görüyoruz:
/evrimagaci.org/public/uploads/images/Makaleler/carbohydrate.png)
Bunların hepsi canlılık dahilinde yapıtaşı olarak ve daha önemlisi, enerji kaynağı olarak kullanılmaktadırlar (bir kısmı yapısal olarak da kullanılmaktadır; örneğin kitin isimli karmaşık şeker yapısı, eklembacaklıların dış iskeletlerinde kullanılan ana malzemedir.
Enerji üretemeyen bir canlının, hayatta kalmak ve üremek için bir aktivite sürdürmesi ve organizasyonunu aktif olarak koruması beklenemez. Dolayısıyla enerji, daha önce de detaylarını gördüğümüz gibi, canlılık için hayati bir kavramdır. Canlılar için bu kadar önemli olan bu molekülleri incelediğimizde, belki de umduğumuzun aksine, pek de sıradışı bir yapı görmüyoruz: 6 adet Karbon atomu (C), 12 adet Hidrojen (H) atomu, 6 adet de Oksijen (O) atomu bir araya gelerek canlıları "canlı" kılan moleküllerden biri olan şekerleri üretebiliyor.
Bu şeker molekülleri, farklı sıra ve biçimlerde bir araya gelerek, daha büyük bileşikleri oluşturabilirler. Örneğin yukarıdaki glukoz ve fruktoz bir araya gelerek, sukroz isimli bir diğer şekeri oluşturabilirler:
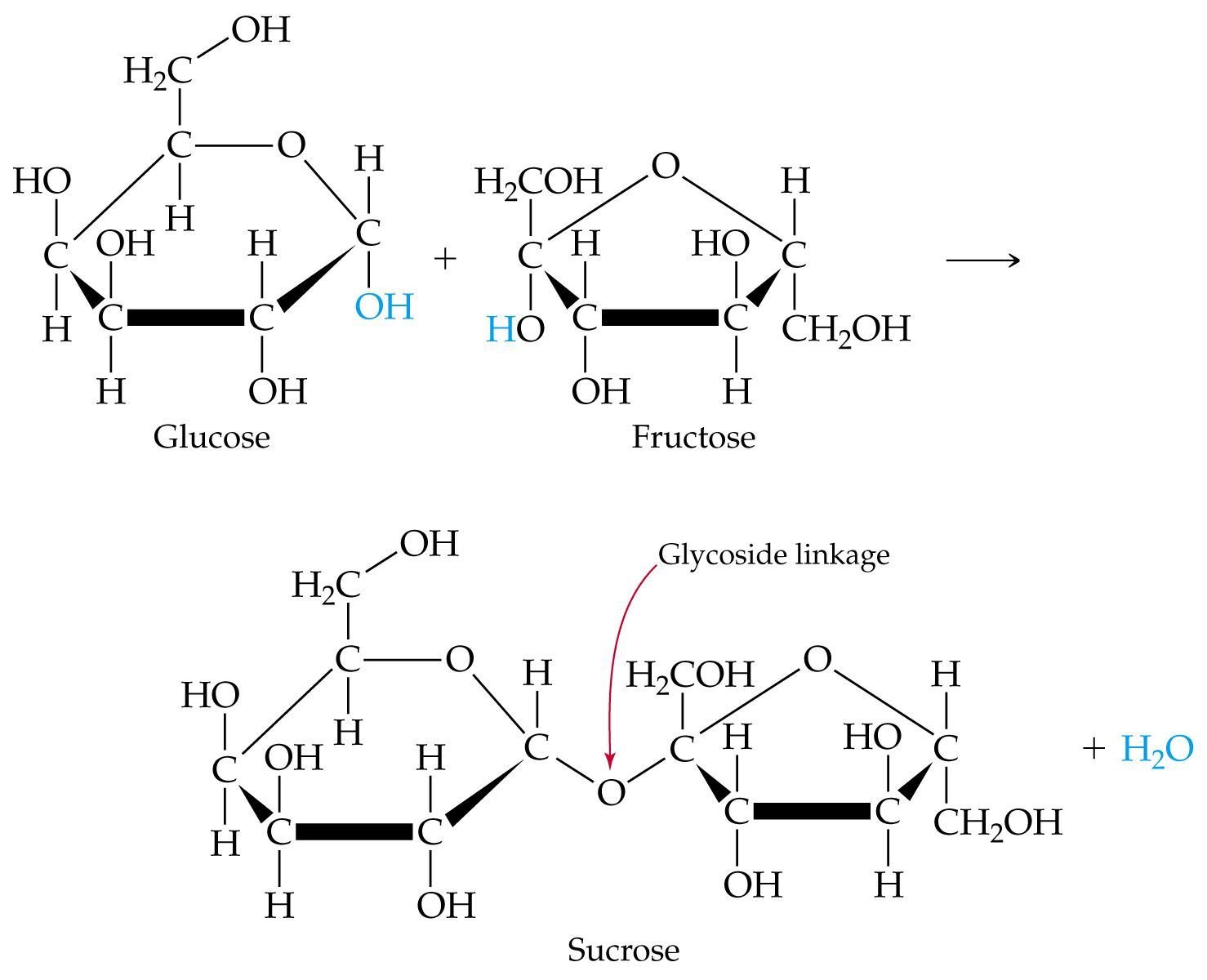
İşte bu şeker molekülleri, daha farklı şekillerde birbirlerine bağlanarak, devasa şeker bileşiklerini oluşturabilirler. Örneğin aşağıda sadece glikozların bir araya gelmesinden oluşan bir glikojen bileşiğini görüyorsunuz:
Aslında maddi destek istememizin nedeni çok basit: Çünkü Evrim Ağacı, bizim tek mesleğimiz, tek gelir kaynağımız. Birçoklarının aksine bizler, sosyal medyada gördüğünüz makale ve videolarımızı hobi olarak, mesleğimizden arta kalan zamanlarda yapmıyoruz. Dolayısıyla bu işi sürdürebilmek için gelir elde etmemiz gerekiyor.
Bunda elbette ki hiçbir sakınca yok; kimin, ne şartlar altında yayın yapmayı seçtiği büyük oranda bir tercih meselesi. Ne var ki biz, eğer ana mesleklerimizi icra edecek olursak (yani kendi mesleğimiz doğrultusunda bir iş sahibi olursak) Evrim Ağacı'na zaman ayıramayacağımızı, ayakta tutamayacağımızı biliyoruz. Çünkü az sonra detaylarını vereceğimiz üzere, Evrim Ağacı sosyal medyada denk geldiğiniz makale ve videolardan çok daha büyük, kapsamlı ve aşırı zaman alan bir bilim platformu projesi. Bu nedenle bizler, meslek olarak Evrim Ağacı'nı seçtik.
Eğer hem Evrim Ağacı'ndan hayatımızı idame ettirecek, mesleklerimizi bırakmayı en azından kısmen meşrulaştıracak ve mantıklı kılacak kadar bir gelir kaynağı elde edemezsek, mecburen Evrim Ağacı'nı bırakıp, kendi mesleklerimize döneceğiz. Ama bunu istemiyoruz ve bu nedenle didiniyoruz.
/old/content_media/0397527d2277fcf3039e8d39c36bc29b.png)
/old/content_media/d7941ca4c22cc26dced9b645553032e3.png)
Bu bileşikler, canlıların yapıtaşı olan hücrelerin pek çok farklı bölgesinde kullanılabilirler. Örneğin enerji üretmek üzere oksijen ile tepkimeye sokulabilirler, bir diğer "hayat molekülü" olan proteinlerle birleşerek hücre zarının yapısına katılabilirler, vs. Örneğin glikoz, hayvanların çoğunun temel enerji kaynağıdır ve hayvanlarda glikoz karaciğerde yukarıda verdiğimiz glikojen şeklinde depolanır. Ancak aynı glikoz, farklı bir bağ yapısı kurarak bitkilerin güçlü hücre duvarını oluşturan selülozu oluşturabilirler. Ya da bir diğer biçimde kimyasal bağ kurarak, böceklerin dış kabuklarında bulunan sert kitin yapısını oluşturabilirler. Genel olarak, şöyle bir tablo çizmek mümkündür:
- Monosakkaritler
- Glikoz: Vücudun temel enerji kaynağıdır.
- Fruktoz: Şekerlerde bulunan, tatlı bir şekerdir.
- Galaktoz: Laktoz ile birlikte, yaygın olarak süt ve süt ürünlerinde bulunan bir şekerdir.
- Disakkaritler
- Sukroz: Çay şekeri veya kristal şeker olarak da bilinen şekerdir; glikoz ve fruktozdan oluşur. Şeker kamışından üretilen şeker sukrozdur.
- Laktoz: Süt şekeridir ve inek sütünün %4-5 kadarını oluşturur. Glikoz ile galaktozdan oluşur.
- Maltoz: Malt şekeri olarak bilinir ve nişastanın amilaz enzimiyle sindirilmesi sonucu oluşur. İki glikozun bir araya gelmesiyle oluşur.
- Polisakkaritler
- Nişasta: Bitkilerde bulunan uzun glikoz zincirleridir. Sindirmesi kısmen daha kolaydır.
- Glikojen: Hayvanların özellikle de kas ve karaciğer dokularında depolanan glikoz zincirleridir. Genellikle kesim sonrasında çok az depo glikojen kalmasından ötürü besin değeri olan bir şeker türü olarak görülmez. Bir hayvan türü olan insan vücudu da fazladan aldığı glikozu kas ve karaciğerde glikojen olarak depolar.
- Selüloz: Yeşil bitkilerin hücre duvarlarında bulunan şeker zinciridir. Beslenme biliminde "fiber" olarak söz edilen zincir budur. İnsanlar selülozu (fiberi) sindiremez; çünkü evrimsel süreçte 20 yaş dişleri ve apandiks organları körelmiştir. Ancak yine de selüloz tüketmenin, sindirim sistemi için birçok faydası vardır: Örneğin daha hızlı tok hissetmenizi sağlar, daha sağlıklı bir sindirim kanalına sahip olmanızı mümkün kılar ve yüksek fiberli diyetlerin doğrudan veya dolaylı olarak kalp hastalıklarını azalttığı ve bazı kanser türlerine yakalanma riskini düşürdüğü düşünülmektedir.
Kısaca her şey kimyasal bağlar ve bunların tipleri ile ilgilidir. Aynı temel bileşikler (ya da "hayat molekülleri"), farklı kimyasal bağların etkisi altında farklı yapılara katılabilirler. Zaten hücrelere bakacak olursanız, "hayat molekülleri"nin farklı bileşimlerinden başka bir şey olmadıklarını göreceksiniz. Kısaca farklı bağlar, farklı ürünler demektir. Bu kadar farklı olasılığın, farklı şekillerde yapıya katılması ve milyarlarca yıldır süren Evrim etkisiyle günümüzdeki canlılık çeşitliliğine ulaşırız.
Karbonhidratlar Nasıl Evrimleşti?
19. yüzyıldan beridir, şekerlerin doğal süreçlerle oluşabileceğini ve ne tür kimyasalların, hangi şartlarda tepkimesinin şekerleri oluşturacağını net bir şekilde bilmekteyiz. Bu konuda, daha 1861 yılında Alexander Butlerow tarafından yapılan deneyler, şekerlerin oluşumuna ışık tutmuştur. Aldehit ismi verilen kimyasalları yüksek sıcaklıkta ve katalizör kimyasallar etkisi altında bırakan Butlerov, formoz tepkimesi adı verilen bir tepkimeyi gerçekleştirerek basit şekerleri yaratmayı başarmıştır.
Deneyde yapılan, basitçe, formaldehit moleküllerinin yaklaşık 100oC sıcaklıkta kalsiyum hidroksit veya kalsiyum karbonat ile katalize etmektir. Bunun sonucunda ilk etapta glikoaldehitler, sonra D-gliseraldehit ve dihidroksiaseton oluşmaktadır. Bu şekilde devam edilen deneyde D-gliseraldehit ve glikolaldehit molekülleri tepkimeye girerek, riboz gibi 5 karbonlu basit şekerleri üretmiştir. Benzer şekilde, D-gliseraldehit ile dihidroksiaseton moleküllerini karıştırırarak D-glikoz ve D-galaktoz gibi 6 karbonlu basit şekerleri yaratmayı başarmıştır. Tüm bu tepkimelerin bir şemasını aşağıda görmek mümkündür:
/evrimagaci.org/dosyalar/fotograflar/ozgun/62/3585_62_07_evow_ch04.jpg)
Bu şekilde sürdürülen deneyler, canlılığın ilk olarak başladığını sonradan keşfettiğimiz, okyanus tabanlarındaki volkanik bacalar ve etrafındaki kimyasalların keşfiyle daha da isabetli sonuçlar vermeye başladı. Çünkü o ortamların yeniden modellenmesi, buralarda canlılık için gerekecek kimyasalların nasıl sentezlenmiş olabileceğini anlamamızı sağladı. Sadece bu bölgelerde, okyanus tabanlarında bulunan kimyasalların deneylerde analiz edilmesiyle, canlılığı oluşturacak tüm kimyasalların yaratılmasının mümkün olduğu gözlendi.
Örneğin 1989 yılında Alman biyolog Egon T. Degens tarafından yapılan bir araştırmada, formaldehit ile kaolin kimyasallarının 100oC gibi bir sıcaklıkta kalsiyum fosfat ile tepkimesi sonucu basit bir şeker olan D-ribozun tamamen doğal biçimde oluşabileceği gösterildi. Bunun haricinde, aynı deneyde, az sonra değineceğimiz adenin gibi nükleotitleri ve fosfolipitleri de üretebilmiştir.
1960 yılında Mayer ve Jaschke tarafından yapılan bir deneyde, %2'lik formaldehit (0.67 M), kalsiyum karbonat bulunan ortamda geridöndürme (İng: "reflux") tepkimesine maruz bırakılmıştır ve bunun sonucunda ribüloz şekeri üretilebilmiştir. 1967 yılında Reid ve Orgel tarafından deney tekrarlanmış ve kalsiyum karbonatın bu formoz tepkimesinde katalizör etkisi gösterdiği doğrulanmış; ancak kağıt kromatografisi yoluyla tespit edilen ribülozun varlığı doğrulanamamıştır. Ancak ikili, yaptıkları deneyde 0.5 M formaldehitin kalsiyum karbonat veya karbonat-apatit varlığında %40 oranında şeker üretebildiğini göstermişlerdir. Öyle ki, 0.01 M kadar düşük molaritelerde bile şeker üretmek mümkün olmuştur. Aynı deneylerde, yaklaşık 24 saat içinde tepkimeden uzaklaştırılması gerektiğini, aksi takdirde süregelen tepkimenin üretilen ürünleri bozmaya başladığı da gösterilmiştir - ki bu durum, okyanus dibindeki volkanik bacalardaki süreğen akıntılarda bu tepkimelerin oluşup, ürünlerin uzaklaştırılmasının avantajlarına işaret ediyor olabilir.
1967 yılında Gabel ve Ponnamperuma, kaolinit, illit ve alüminyum gibi mineral ve elementlerin varlığında, yukarıdaki tepkimelerdeki ortamın aksine, bazik değil de tamamen nötr ortamlarda bile heksoz, pentoz, tetroz ve trioz şekerlerin oluşabildiğini, hem de 0.01 M kadar düşük molaritelerde bile oluşabildiğini göstermişlerdir. 1972'de Cairns-Smith, 0.13 M formaldehit ile geridöndürme tepkimelerini test etmiş ve kuartz, kalsit ve galena gibi çok sayıda mineralin şeker oluşumunu katalizleyebildiğini göstermiştir.
1993 yılında Schwartz ve Graaf, 0.1 M formaldehitin, ısıtılması halinde Dünya'da yaygın olarak bulunan çok sayıda mineralin etkisi altında katalizlenebildiğini ve otokatalitik (kendi kendinin üretimini hızlandıran) formoz tepkimesinin elde edilebildiğini göstermiştir. Bu tepkimenin kalsiyum iyonlarına veya önceki deneylerde gereksinim olduğu sonucuna varılan güçlü bazik bir ortama ihtiyacı olmadığını da göstermişlerdir. Bu tepkime sonucunda oluşan şekerler seçici değildir; ancak Dünya atmosferindeki formaldehitin fotokimyasal sentezi yoluyla pentaeritritole dönüşümü fazlasıyla seçicidir ve bu süreçte oluşan karbonhidrat oluşumu, yaşamın başlangıcındaki şekerlerin inorganik moleküllerden oluşumunu açıklayabilir.
2020 yılında Haas ve arkadaşları; hidroksitler, karbonbatlar, silikatlar, mikalar, zeolitler, killer, olivinler, fosfatlar ve fosfitler gibi muazzam bir mineral çeşitliliği içerisinde, glikoaldehitten şeherlerin mekanokimyasal bir şekilde oluşabileceğini göstermişlerdir. Üstelik bu tepkimeler oldukça kısa sürelerde yaşanmış ve düzenli bir şekilde monosakkaritleri üretmeyi başarmıştır. Mineral bolluğuna bağlı olarak aldozlar, ketozlar ve hatta spesifik şekerlerin üretimi kontrol edilebilmektedir. Su ortamında değil de atmosferik şartlarda yapılan deneylerde, bu sürecin oksijen varlığından da bağımsız olduğu, yani oksijen olsaydı bile tepkimenin devam edebileceği gösterilmiştir. Benzer şekilde, katyon kompozisyonlarına bağlı olarak tepkimenin seçiciliği geniş bir aralıkta değişebilmektedir ve bu da şekerlerin erken Dünya'da oluşabilmesi için potansiyel kimyasal çeşitliliğini yansıtmaktadır. Araştırmanın yazarları, çalışmalarını şöyle özetliyor:
Genel olarak, mekanokimyasal formoz tepkimesi, erken Dünya koşullarında olan jeokimyasal şartlar altında şekerlerin (monosakkaritlerin) oluşabilmesi için sağlam bir sentez yolağı sunmaktadır. Dahası, katı-faz tepkimesi, şekerlerin su olmayan ortamda da oluşabildiğini göstermekte ve bu sayede Dünya-dışı şeker oluşumuna da kapı aralamaktadır. Bu durum, içinde su bulunmayan meteoritlerde şeker bulunduğunu gösteren yakın geçmişteki araştırmaların bulgularını izah etmektedir.
Proteinler: Yapıları, Özellikleri ve Oluşumları
Proteinler genellikle kas dokusu ile ilişkilendirilir; ancak canlılığı oluşturan bütün doku ve organların yapısında proteinler görev alır. Proteinler, aminoasit denen daha ufak moleküllerin uç uca, üst üste, yan yana peptit bağı adı verilen bir bağ türüyle bağlanması sonucu oluşan bir molekül kompleksidir. Peptit bağı, aminoasitlerin su kaybetmesi (dehidrasyonu) ile oluşan, kovalent yapılı bir bağdır.
Öyle ki, aminoasitler ile proteinler arasında "ara geçiş kimyasalları" olarak görebileceğimiz, peptit isimli kimyasallar da bulunur. Bunlar, ne protein olan ne de tek başına aminoasit olan, polimer varyantlarıdır. Bunların birikimli seçilimi sonucunda daha karmaşık proteinler inşa edilebilir. Hatta peptitlerle proteinler arasında, boyları genelde 100 aminoaside kadar olan polipeptitler vardır.
Aminoasit ve Proteinlerin Yapıları
Şekerlerin ve az sonra göreceğimiz lipitlerin aksine, proteinlerin tamamında karbon, hidrojen ve oksijen atomlarına ek olarak azot atomları da bulunur; önemli bir bölümünde sülfür atomlarına da rastlanır. Aminoasit dediğimiz yapı, amino grubu ile karboksil grubu adı verilen iki kimyasal grubun bağlanmasıyla oluşur. Amino (veya İng: "amine"), "azot içeren" demektir; karboksil ise "karbon içeren" demektir. Aşağıda günümüze kadar süren evrimsel süreçte oluşmuş 20 temel aminoasidi ve bunların kimyasal yapısını görmektesiniz:
/evrimagaci.org/dosyalar/fotograflar/ozgun/62/4376_62_amino-acid-table1.gif)
Burada gösterilenler, canlılığın yapıtaşları arasında olduğu bilinen 20 aminoasittir. Ancak canlılığın yapısına katılmayanları da sayacak olursak, 300'den fazla aminoasit olduğu bilinmektedir. Bunların hepsi aynı yapıya sahiptir ve hepsinde merkezi bir karbon atomu, şunlara bağlanır:
- bir hidrojen atomu,
- alkalin (bazik) bir amino grubu (NH2)
- asidik bir karboksil grubu (COOH)
- değişken bir grup
/old/content_media/7cbe160f7d5e2a0046c3b5a852f72629.jpg)
Görselden görülebileceği üzere, bir aminoasidin de yapısında, diğer moleküllerden farklı bir özellik yoktur. Tek gördüğümüz; karbonlar, oksijenler, hidrojenler ve azottur! Aminoasitlerin içerisinde hem asidik, hem bazik özellikte parçalar bulunduğu için, organizmaların asit-baz dengesini sağlamasında çok avantajlı bir moleküldür.
Aminoasit şemalarında yaygın olarak gösterilen “R” harfi, "radikal" kelimesinin ilk harfidir. Bu harf, değişken uzunlukta ve yapıda bir kimyasal grubu ifade etmektedir; buna yan zincir veya R-grubu denmektedir. Molekülün bu kısmına da çeşitli atomlar bağlanarak, birbirinden farklı aminoasitleri oluştururlar. Bu grubun esnekliği, aminoasit çeşitliliğinin kökeninde yatan kimyasal kaynaktır; çünkü bu parça farklı boyutlarda olabilir, polar veya apolar olabilir ve tüm bu nitelikleri sayesinde aminoasitlere bambaşka özellikler kazandırabilir. Örneğin sistein ve metiyonin isimli iki aminoasitte bu yan zincir, sülfür de içermektedir. Sülfür, hidrojen bağlarına katılmaz; ancak diğer tüm aminoasitlerde hidrojen bağları vardır ve sadece bu basit varyasyon bile, bu iki aminoasidi içeren proteinlerin yapısını köklü bir şekilde değiştirebilir. Yani aminoasitlerde gördüğümüz bu geniş çeşitlilik, kimyasal evrim ve canlılığın başlangıcı açısından büyük öneme sahiptir.
Proteinlerin Oluşumu ve Yapısal Formlarının Önemi
Bu aminoasitler, farklı şekillerde uç uca birleşerek, milyonlarca farklı proteini oluşturabilirler: Bu 20 aminoasitten bir kısmını içeren sadece 20 aminoasitlik zincir, bildiğimiz en küçük protein olan TRP-Cage proteinini oluşturabilirken, aynı 20 aminoasitten yüzlercesi ve binlercesi bir araya gelerek, hücrelerimizde bulunan devasa proteinleri oluşturabilirler. Örneğin vücudumuzda bulunan 27.000-33.000 aminoasitli titin proteini, bildiğimiz en büyük proteinlerden birisidir; ancak canlılardaki aminoasitlerin çoğu, genellikle birkaç on ila birkaç yüz aminoasidin bir araya gelmesiyle oluşur. Yani aynı aminoasitler, farklı şekillerde bir araya gelerek, inanılmaz bir protein çeşitliliği oluşturmaktadır. Bu çeşitlilik, yaşamın çeşitliliğin özüdür! Örneğin aşağıda bir G-Proteini görüyorsunuz:
/evrimagaci.org/public/uploads/images/Makaleler/1b9x_opm.png)
Bu protein yapısında yüzlerce aminoasit, farklı sıra ve sayılarda kullanılmaktadır (yukarıdaki temsili bir 3 boyutlu çizimdir, dolayısıyla aminoasitler ayrı ayrı gözükmemektedir). Bu sıraların ve sayıların değişmesi, farklı özelliklerde proteinlerin üretilmesi, bu da farklı protein moleküllerinin farklı işlevlere sahip olabilmesi demektir. Bunu, Türkçede bir cümle oluşturmaya benzetebilirsiniz. Bu benzetimle ilgili detaylı bir yazımızı buraya tıklayarak okuyabilirsiniz.
Proteinlerin şekilleri, onların nasıl çalışacağını doğrudan belirler. Yani proteinleri adeta bir "alet" gibi düşünebilirsiniz. Nasıl ki bir çorba içmek için çatal, bir biftek yemek için kaşık kullanamazsınız (veya kullansanız da pek iyi çalışmaz), proteinlerin de şekilleri, onların neler yapmakta kullanılabileceğini belirler. Bu nedenle proteinlerin şekil ve yapı çeşitliliği büyük öneme sahiptir.
Proteinleri oluşturan aminoasitlerin bir araya gelmesiyle birincil yapı dediğimiz polipeptit zincirleri oluşur. Birincil yapıyı bir arada tutan, kovalent bağlardır. Bu zincir, kendi üzerine farklı şekillerde katlanarak alfa-heliks veya beta-katlanmış plaka adı verilen, ikincil yapı olarak da bilinen şekilleri oluştururlar. Bu ikincil yapı, aminoasitler arasındaki hidrojen bağlarıyla bir arad tutulur. İri proteinlerin bu katlı şekli, tekrar kendi üzerine katlanarak üçüncül yapı dediğimiz bir şekli oluştururlar. Hatta bazı proteinler öylesine iridir ki, kendilerini oluşturan aminoasit gruplarını "alt birim" olarak bilinen parçalara bölmemiz mümkündür ve bu parçaların birbiriyle etkileşimi, dördüncül yapı adını verdiğimiz, protein fonksiyonlarını doğrudan etkileyen bir yapıyı oluşturur.
Yani proteini oluşturan aminoasitlerin yapısı, sayısı ve dizilimleri, proteinlerin tam olarak ne şekle sahip olacağını ve dolayısıyla ne işler yapabileceğini belirler. Örneğin kaslarımızı oluşturan uzun ve ince proteinler, bu şekilleri sayesinde uzayıp kısalabilirler; öte yandan, kemiklerimizi oluşturan uzun kolajen proteinleri, kemiklerimizdeki minerallerin birikebileceği bir kalıp görevi görürler. Bu tür uzunlamasına proteinlere fibröz proteinler deriz.
Öte yandan küresel (globüler) proteinler, isimlerinden de anlayabileceğiniz gibi, daha küresel bir şekle sahiptir. Bu şekilleri sayesinde tepkimeye girmeye çok daha meyillidirler ve çoğu zaman hidrofiliktirler, yani suyu severler (ortamda su molekülleri varsa, ona doğru çekilirler). Örneğin kan hücrelerimizde bulunan hemoglobin proteini, bu yapıda bir proteindir.
Bir proteinin şeklini bozmak için onu ısıtmanız veya asidik veya bazik kimyasallara maruz bırakmanız gerekir. Bunun sonucunda denatürasyon denilen bir süreçten geçerek, proteinin az önce sözünü ettiğimiz dördüncül, üçüncül, ikincil ve kimi zaman birincil yapısı parçalanır. Yapısal şeklini yitiren proteinler, artık görevlerini yerine getiremezler (işlevlerini de yitirirler). Bunun gündelik yaşamdan en bilindik örneği, süte limon suyu damlatmanız halinde kısa bir süre içinde oluşan kararmadır.
Proteinlerin Görevleri
Proteinler, temel olarak her yerde kullanılabilen, çok önemli, son derece istikrarlı (stabil) moleküllerdir. En önemli görevleri arasında enzimleri oluşturmak ve diğer tepkimelerin hızlarını kat be kat arttırmak bulunur. Çünkü doğadaki birçok kimyasal tepkime oldukça yavaştır; ancak ortamda enzimlerin veya katalizörlerin bulunması halinde bu tepkimeler çok daha hızlı gerçekleşebilir. Eğer vücudumuzda protein yapılı enzimler bulunmasaydı, vücudumuzun şu andaki şekliyle işlemesi mümkün olmazdı (tabii bu tür kimyasal ön koşullar altında, bambaşka yapıların evrimleşebileceği de iddia edilebilir).
Protein yapılı enzimlerde asıl iş, enzimin aktif bölge adı verilen kısmında gerçekleşir. Her enzim, çok kısıtlı sayıda (neredeyse her zaman 1 adet) tepkimeyi hızlandırabilir; çünkü az önce de söylediğimiz gibi proteinlerin yapısındaki her türlü değişim, onların fonksiyonunu da az çok etkilemektedir. Buna, enzim spesifitesi adı verilir. Bu özellik çerçevesinde, sadece belirli bir şekle ve elektrik yüküne sahip olan kimyasallar enzim ile bağ kurabilir.
Bir enzimin, hızlandıracağı kimyasal tepkimede bağlandığı maddeye substrat adı verilir. Bu ikili birbirine bağlandığında, enzim-substrat kompleksi üretilmiş olur. Enzimler, sihirli moleküller değildir; en nihayetinde, diğer kimyasal maddelerin oryantasyonunu (duruş yönünü) ve kimi zaman fiziksel yapısını (konformasyonunu) değiştiren moleküllerdir. Bir enzim, bir substratı, kimyasal tepkimeye daha açık hale getirir; bu sayede normalde o kimyasal madde daha yavaş tepkime geçirirken, enzim varlığında daha hızlı bir şekilde tepkimeye girebilir. Tepkime sonrasında enzim, yapısı değişen substrata bağlanamaz ve enzim-substrat kompleksi dağılır. Böylece o enzim, bir diğer substrata bağlanmak üzere boşa çıkmış olur ve bu sayede enzimler, substrat var olduğu sürece, neredeyse durmaksızın kimyasal tepkimeleri hızlandırmaya devam edebilirler.
Bu açıdan, enzimatik görevi olan proteinler ilk defa evrimleştikten sonra, kimyasal evrimin ne kadar büyük bir hız kazandığı da anlaşılır olacaktır. Bu noktada, tepkimeleri hızlandıran tek unsurun enzimler olmadığını, kimi zaman basit inorganik katalizörlerin de kimyasal tepkimeleri hızlandırabildiği hatırlanmalıdır. Bu katalizörlerin etkisi altında aminoasitler ve proteinler evrimleşmiş, bu proteinlerin faaliyetleri sayesinde diğer kimyasal süreçler hızlanarak, evrime hız katmıştır.
Ancak proteinlerin tek görevi enzimatik faaliyet değildir. Vücudumuzdaki neredeyse her işlev, proteinler sayesinde yapılır. Çünkü genetik kodlarımız, proteinlerin üretimini kodlamaktadır ve bu sayede aklınıza gelebilecek her özelliğimizi kazanırız. Ayrıca proteinler, hücrelerin yapısına da katılarak önemli iletişim ve yapı görevleri üstlenebilirler. Derinizin üst tabakasındaki keratin yapısı, proteinlerden inşa edilir. Derinizin dermis tabakasındaki, kemiklerinizdeki ve beyninizin menenj adı verilen zarındaki kolajen, proteinlerden inşa edilir. Sindirim kanalımızdaki sindirim enzimleri, savunma sisteminizdeki antikorlar, sinir sisteminizdeki nörotransmiterler, hormonal sisteminizdeki hormonların önemli bir bölümü, peptit-temelli proteinlerdir. Tüm bunlar, aminoasitlerin farklı kombinasyonlarından ötürü proteinlerin de farklı özelliklerde olabilmesinin bir sonucudur. Bu sebeple canlılığı, "proteinlerin işlevlerinin bir toplamı" olarak görmek çok da isabetsiz bir düşünce olmayacaktır.
Aminoasitler Nasıl Evrimleşti?
Peki proteinleri oluşturan aminoasitler, kendilerinden önce gelen inorganik moleküllerden nasıl oluşmuş olabilir?
Her ne kadar aminoasitlerin kimyasal tepkimelerle, dolayısıyla kendiliğinden oluşabileceklerini ispatlayan deneyler 19. yüzyılın başlarına, Alman kimyager Friedrich Wöhler'e kadar dayansa da; başarılı bir biçimde, laboratuvar ortamında ilk defa 1850 senesinde Adolphe Strecker tarafından bir aminoasit üretilmiştir. Strecker, yine okyanus tabalarında bulunduğunu bildiğimiz (o zamanlarda bu bilinmiyordu) asetaldehit, formladehit, amonyak ve hidrojen siyanit kullanarak alanin ve glisin isimli bir aminoasitleri doğal yollarla sentezlemeyi başarmıştır. Bugün bu tepkimeler Strecker Sentezi olarak bilinmektedir (aşağıda gösterilmiştir). Günümüzde bu tepkime ve benzerlerinin okyanus tabanlarındaki volkan bacaları etrafında, kendiliğinden olduğunu ve aminoasitleri oluşturduğunu biliyoruz.
/evrimagaci.org/dosyalar/fotograflar/ozgun/62/3596_62_streck4.gif)
Sadece bu da değil. 1913 yılında Walther Löb ve Oskar Baudish potasyum siyanür ve formaldehit kullanarak, mor ötesi ışınlar ve elektrik etkisi altında glisini üretmeyi başardı. Hatta sonradan, ilkel atmosferik koşullarda karbonmonoksit ve amonyak gazlarının elektrik yükü altında tepkimesiyle de formamidinin sentezlenebileceğini ispatladılar.
Günümüzde, canlılığın başlangıcı için gereken tüm kimyasalların su içerisinde oluşmadığını ve atmosferde de birçok kimyasalın oluştuğunu biliyoruz. Daha sonradan okyanuslar üzerine yağmurlarla veya başka yollarla çöken bu kimyasallar, okyanus tabanlarında birikmeye başlamış ve canlılığın yapısına katılmıştır. Dolayısıyla canlılığın başlangıcını sadece okyanus tabanlarıyla sınırlı tutmak doğru olmayacaktır. Bunlara daha sonradan geleceğiz.
Aminoasitlerin doğal süreçlerle oluşabileceği konusuna odaklanan tek bilim insanları bunlar değildir. Yüzlerce biyokimyager bu konuda uzmanlaşarak canlılığın sırlarını çözmeye çalışmışlardır. Bunlardan en meşhur olanları şüphesiz öncelikle Alexander Oparin, sonrasında ise Stanley Miller ile Harold Urey'dir. 1953 yılında ilk defa yapılan Miller-Urey Deneyi, günümüzde halen yankılarını sürdürmektedir. O dönemden sonra yapılan 460'tan fazla denemede, sadece tüm aminoasitler değil, Hayat Molekülleri'nin neredeyse tamamı laboratuvar koşullarında elde edilebilmiştir.
Bu deneyi ve detaylarını bir başka yazımıza sakladığımız için, burada detaylarına pek girmeyeceğiz. Ancak ilk yapılan ve temel bazı hataları bulunan (sonradan diğer deneylerde düzeltilmiştir) Miller-Urey Deneyi'nde üretilen yapılar şunlardır:
- Karboksisilik Asitler
- Formik asit
- Asetik asit
- Propiyonik asit
- Düz ve dallı yağ asitleri (C4-C10)
- Glikolik asit
- Laktik asit
- Susinik asit
- Nükleik Asit Bazları
- Adenin
- Guanin
- Ksantin
- Hipoksantin
- Sitozin
- Urasil
- Amino Asitler
- Glisin
- Alanin
- α\alpha-aminobütrik asit
- Valin
- Lösin
- İzolösin
- Prolin
- Aspartik asit
- Glutamik asit
- Serin
- Treyonin
- Şekerler
- Düz ve dallı pentozlar ve hekzozlar
Üstelik tüm bunların oluşumu sadece 6 gün sürmüştür! 2012 yılında Harold Urey'in laboratuvarında sakladığı bazı deney tüpleri açığa çıkarılmıştır. Yapılan analizlerde, 1953 senesinden bu yana bekleyen tüplerde tüm aminoasitlerin, şekerlerin tamamının, nükleik asitlerin ve canlılığın yapısına doğrudan katılmayan birçok organik molekülün kendiliğinden oluştuğu görülmüştür. Tahmin edilebileceği gibi bu deneylerde zaman arttıkça, ürünler de artmaktadır. Unutmayınız ki yapılan deneyler, yaklaşık 400-600 milyon yılda oluşan canlılığın temellerini, sadece birkaç gün ve haftada elde etmeyi hedeflemektedir. Buna rağmen, çok başarılı sonuçlar elde edebilmektedirler!
Daha sonradan yapılan deneylerde, aminoasitlerin doğal süreçlerle bir araya gelerek proteinleri oluşturabileceği de ispatlanmıştır. Örneğin Sidney Fox'un yaptığı deneylerde 150oC sıcaklıkta 15 gün kadar bir süre içerisinde 23 aminoasit uzunluğunda proteinlerin oluştuğunu gözledi. Fox, bu deneylerinde sodyum klorür, bikarbonat, aspartik asit, glutamik asit, karbonik asit, amonyum klorür gibi kimyasallar kullanmıştır. Kendisinden sonra yapılan deneyler de, Fox'un çalışmalarını doğrulamış ve hatta daha uzun yapılı proteinlerin de birkaç haftada kendiliğinden oluşabileceğini ispatlamıştır.
Lipitler: Yapıları, Özellikleri ve Oluşumları
Lipitler (yağlar), çoğunlukla hidrokarbon adı verilen, hidrojenli ve oksijenli moleküllerden oluşan, oldukça çeşitli bir molekül grubudur. Bu moleküllerde oksijen atomları, genellikle molekülün dış kısmında ve az sayıda bulunur. Ayrıca bu hidrokarbon yapısı, lipitlerin tamamını hidrofobik, yani sudan nefret eden yapıda kılmaktadır; bir diğer deyişle, bu moleküller su moleküllerinin olduğu durumda o moleküllerden uzak durmaya çalışırlar. İşte tam da bu nedenle su ile yağları karıştıracak olursanız, gerçek bir karışım elde etmezsiniz; bunun yerine, emülsiyon adı verilen, pek düzgün karışmayan sıvıları barındıran bir katman elde edersiniz.
Lipit Çeşitleri
Lipitleri genel olarak üç gruba ayırarak incelemek mümkündür:
- Trigliseritler: Besinlerle aldığımız en yaygın yağ grubudur ve organizmaların yapısında en yaygın bulunan yağ molekülü de budur. Aslında yağ olarak ifade ettiğimiz lipitler, bu tür lipitlerdir. Dolayısıyla hayat molekülleri açısından önemli olanlar da bunlardır. Bunlar, iki parçadan oluşurlar:
- Gliserol: Trigliseritlerin omurgası konumunda olan, 3 karbondan oluşan, çok kritik bir moleküldür.
- Yağ Asitleri: Bir ucunda bir karboksil grubu, diğer ucunda bir metil grubundan oluşan bu moleküller, gliserolü oluşturan üç karbonun her birine bağlanan yapılardır. Yağ asitlerini de iki genel gruba ayırmak mümkündür:
- Doymuş Yağ Asitleri: Eğer bu zincir boyunca ikili karbon bağları yoksa, dolayısıyla oluşabilecek maksimum sayıdaki hidrojen bağı oluşmuşsa, bunlara doymuş yağ asidi denir. Bunlar; düz ve sağlam yapılı zincirlerdir, birbirlerine sıkı sıkıya bağlanırlar ve dolayısıyla oda sıcaklığında katı veya yarı-katı halde bulunurlar. Tereyağı (margarin) ve domuz yağı, en blindik örnekleridir.
- Doymamış Yağ Asitleri: Hidrojen bağları yerine ikili karbon bağları olan bu tür yağ asitleri, düz yapılı değildir ve bu nedenle birbirlerine sıkı sıkıya bağlanamazlar. Buna bağlı olarak oda sıcaklığında sıvıdırlar. Bitki yağları, tekli ya da çoklu doymamış yağ asitlerini içeren meşhur yağlardır.
/old/content_media/86e7c04668ffc18db1e6291cdfe4c4a4.png)
- Fosfolipitler: Hücrelerin sitoplazmalarını çevreleyen zarı oluşturan moleküller fosfolipitlerdir. Kutuplu (polar) ve fosfat içerikli kafa kısımları ile, kutupsuz olan kuyruk kısımları vardır. Fosfolipitlerin kuyruk kısmı hidrofobiktir ve diğer yağlarla etkileşime geçebilir; kafa kısmı ise hidrofiliktir ve su ile etkileşime geçer. Bu özellikleri dolayısıyla emülgatör olarak da bilinen fosfolipitler, canlılığın cansızlıktan kimyasal evrimi için son derece önem arz etmektedir: Fosfoliptiler, yapıları gereği su içerisinde küresel, çift katmanlı bir zırh oluşturabilirler. Bu zırh, fizik yasaları etkisiyle, kendiliğinden oluşabilmektedir ve oldukça istikrarlıdır. İlk hücresel yapıların bu zırh içerisinde başladığı düşünülmektedir ve bu düşünce, günümüzdeki bütün hücrelerin zar yapılarının yağ temelli olmasıyla desteklenmektedir. Yazı dizimizin ilgili yazısında lipitlerin yaşamın başlangıcı için önemine daha detaylı bir biçimde gireceğiz; dolayısıyla burada sadece genel bir özet vermek istedik.
/old/content_media/39ba80e45d12cd7085849190a3911aec.jpg)
- Steroidler: 4 hidrokarbon zincirinin diğer atomlara ve moleküllere bağlanmasıyla oluşan steroller (veya steoridler), özellikle de kolesterol örneğinde olduğu gibi vücut içerisindeki fonksiyonların düzgün işleyebilmesi için büyük öneme sahiptir. Kolesterol gibi steroidler birçok hormonun yapıtaşıdır ve hormonlar, vücutta sentezlenerek daha uzak bölgelerdeki işlevlerin yerine getirilmesini sağlayan kimyasal moleküllerdir. Steroidler de hücre zarının yapısına katılarak, hücre içine giren ve hücre içinden çıkan maddeleri regüle ederler.
/old/content_media/d892a7bad52475b273f2256934f975c2.png)
Trigliseritlerin Diğer Görevleri
Trigliseritler, vücudumuz için en önemli enerji kaynaklarından birisidir. Örneğin siz uyurken veya dinlenirken, enerjinizin çoğu şekerlerden değil, yağ deponuzda (adipoz dokularınızda) birikmiş trigliseritlerden karşılanır. Ayrıca trigliseritler; bahçıvanlık veya yürüyüş gibi uzun soluklu ve yavaş fiziksel faaliyetleri de yapabilmenizi sağlayan enerji kaynaklarıdır. Daha yoğun enerji isteyen faaliyetlerde şekerler yakıt görevini devralır; ancak bunlarda bile yağlar önemli bir enerji kaynağı olmayı sürdürürler.
Ayrıca besinlerle aldığınız yağlar, gıda emilimine yardımcı olur ve polar-olmayan, yağ içinde çözünebilir A, D, E ve K vitaminlerinin vücutta taşınmasını sağlar. Buna ek olarak yağlar, birçok organizmanın vücudunu dış faktörlere karşı koruyarak, daha iç kısımlardaki organların faaliyetlerini sürdürebilmesine önemli bir role sahiptir (ve vücut sıcaklığımızı da korumamızı sağlar).
Gliserol Nasıl Evrimleşti?
Burada değinmek istediğimiz konu ise, lipitlerin oluşumundaki kilit nokta olan gliserolün doğal yollarla nasıl oluşabileceğini açıklamaktır. Bu konuda yapılan ilk çalışma, 1971 yılında Takashi Mizuno ve Alvin Weiss tarafından yapılmıştır. Yapılan deneylerde D-gliseraldehit ile formaldehit, düşük sıcaklıkta sodyum hidroksitin katalizörlüğünde tepkimeye girerek sadece 30 dakika içerisinde gliserol oluşabilmiştir. Üstelik sadece gliserol de değil, riboz ve glikoz gibi şekerler de bu tepkime sırasında oluşmuştur. Günümüzde bu tepkimeler Cross-Cannizzaro Tepkimesi olarak bilinmektedir. Aşağıda bu tepkime görülmektedir:
/evrimagaci.org/dosyalar/fotograflar/ozgun/62/3597_62_crosscannizzaroreaction.png)
Kimyasal Evrim Açısından Organik Bileşikler ve Hayat Molekülleri
Bizi "canlı" kılan moleküllerden hangisinin ilk olarak oluştuğunu kestirmek oldukça güçtür; zira yapılacak tahminler, en nihayetinde spekülasyondan öteye gitmeyecektir. Bu tür moleküler oluşumlar çoğunlukla rastlantısal bir doğaya sahiptir ve tamamen çevre koşullarına bağlı olarak gerçekleşirler. Ancak bu konuda yapılacak en iyi tahmin, hepsinin birbirine yakın zamanlarda oluşmuş olduğudur; çünkü canlılığın başlangıcına yönelik modern laboratuvar deneylerinde gözlediğimiz budur: Yaşamın temeli olan organik bileşiklerin hepsi, deney tüplerinde neredeyse eş zamanlı olarak oluşmaktadır.
Yaşamın başlangıcını anlayabilmek için, bu sıra büyük bir öneme sahip değildir. Çünkü kalıtım materyali görevini üstlenen nükleotitler, enerji ve yapıtaşı olma konusunda önemli görevi olan karbonhidratlar, düzenleyici ve istikrarı sağlayıcı yapılarından ötürü proteinler ve esneklik, koruma ve barındırma gibi özelliklerinden ötürü lipitler, farklı zamanlarda oluşmuş olsalar da, canlılığın evrimleştiği zaman aralığında çoktan oluşmuşlardı ve halihazırda serbest halde bulunmaktaydılar. Cansızlıktan canlılığın evrimini anlayabilmek için önemli olan, canlılığın yapısına nasıl katıldıkları ve yeni evrimleşen bu sistem üzerinde ne tür etkileri olduğudur.
Bu noktada, "canlılık" tanımına yeniden göz atmakta fayda var. Kimyada "organik moleküller", canlıları cansızlardan pratik olarak ayırmak için kullanılabilirler; çünkü bahsettiğimiz gibi canlıların tamamında organik moleküller bir arada bulunur, cansızlarda ise bulunmak zorunda değildir. Ancak bu, çok verimli bir kategorizasyon değildir. Çünkü canlılarda elbette inorganik moleküller de bulunmaktadır; örneğin akciğerlerimizin %83'ünü, vücudumuzun %60'ını oluşturan su, inorganiktir. Benzer şekilde, cansız yapılarda da belli başlı organik moleküller bulunabilir. Örneğin genellikle karbon içeren moleküller "organik" olarak sınıflandırılır (her ne kadar karbondioksit gibi bu tanıma dahil edilmeyen moleküller olsa da); örneğin 1828 yılında bile laboratuvar şartlarında, hiçbir canlı olmaksızın üre sentezlemek mümkün olmuştur. İlerleyen kısımlarda daha detaylıca göreceğimiz üzere, organik moleküller, inorganik moleküllerden, canlılığa ihtiyaç duymaksızın sentezlenebilmektedir. Buna rağmen, belli bir oranın üzerinde organik yapılardan oluşan varlıkların canlı olması oldukça muhtemeldir.
Oldukça kesin olan bir gerçek vardır: Evrim, çoğu zaman basitten karmaşığa doğru gerçekleşmektedir. Bu, aslında evrimle ilgili bir durum değildir; termodinamiğin (ve fiziğin) temelinde yatan entropiyle ilgili bir konudur.Evrim, yeni bir sistemi bir anda "yaratamaz" (yoktan var edemez); ortada halihazırda var olan materyali ve çeşitleri değiştirerek kullanır. Dolayısıyla, canlılığı cansızlıktan ayıracak olan hayat molekülleri de, esasında kendilerinden önce oluşan inorganik veya organik bileşiklerden, kimyasal yollar, süreçler ve tepkimelerle evrimleşmiş yapılardır. Var olan kimyasal yapılar, ortama uygunlukları açısından doğa tarafından bir varlık sınavına tabi tutulurlar. En uyumlu ve istikrarlı olanlar varlıklarını daha uzun süreler korur, diğerleri ise parçalanarak dağılır ve yok olur. İşte biz buna, basitçe, Kimyasal (Doğal) Seçilim adını vermekteyiz. Unutmamak gerekir ki, sadece istikrarlı ve düzenli olanlar ortama en uygun olanlar olmak zorunda değildir. Kimi ortam ve çevre şartlarında istikrarsızlık ve hızlı bozunma da, bu süreçlerin içerisinde bulunduğu daha büyük yapıların sürekliliği açısından avantaj sağlayabilir. Önümüzdeki yazılarda bunları detaylıca ele alacağız.
Dolayısıyla bir protein molekülü, yağ molekülü, nükleotit molekülü, vb. oluşmadan önce, bunları oluşturan yapıtaşları oluşmalıdır - ki bunlar daha küçük, daha basit yapıda moleküllerdir. Daha da derinlere inerek, molekülleri oluşturan yapılara bakacak olursanız, tam da beklendiği gibi atomları görürsünüz. Daha da derinlerde atomaltı parçacıklar yatar; ancak bu, şu anda konumuzun dışındadır. Bilmemiz gereken nokta, atomların bir araya gelmesiyle envai çeşit molekülün oluşabildiği ve bu moleküllerden "Hayat Molekülleri" olarak isimlendirilen bir grubun, bazı varlık formlarının "canlılık özellikleri" olarak verdiğimiz özelliklere sahip olmalarını sağladığıdır.
Sonuç
Görülebileceği gibi tüm yaşam molekülleri, çok basit tepkimelerle, kendiliğinden oluşabilmektedir. Dahası, bu tepkimeler için gerekli tüm inorganik altyapı, zaten Dünya'nın oluşumu sırasında gezegenimiz içerisinde bulunmaktadır. Dolayısıyla tek yapılması gereken beklemektir. Tıpkı domino taşlarının yıkılması gibi, zaman içerisinde tepkimeler gerçekleşerek canlılığın temellerini oluşturmuşlardır.
Geriye sadece nükleotitleri oluşturmak kaldı; ancak onlara burada girmeyeceğiz, bir sonraki yazımıza saklıyoruz; çünkü orada, çok daha detaylı olarak işleyeceğiz, akla takılabilecek birçok soruya cevaplar vereceğiz. Hepsini buraya sıkıştırmak istemiyoruz. Ancak şimdiden tahmin edebileceğiniz gibi, nükleotitler de diğer moleküllerden farksızdır, benzer yapılara sahiptirler ve tamamen doğal yollarla, hiçbir dış müdahale olmaksızın oluşabilirler. Bunlara zaten yeri geldiğinde yeniden gireceğiz.
Evrim Ağacı'nda tek bir hedefimiz var: Bilimsel gerçekleri en doğru, tarafsız ve kolay anlaşılır şekilde Türkiye'ye ulaştırmak. Ancak tahmin edebileceğiniz gibi Türkiye'de bilim anlatmak hiç kolay bir iş değil; hele ki bir yandan ekonomik bir hayatta kalma mücadelesi verirken...
O nedenle sizin desteklerinize ihtiyacımız var. Eğer yazılarımızı okuyanların %1'i bize bütçesinin elverdiği kadar destek olmayı seçseydi, bir daha tek bir reklam göstermeden Evrim Ağacı'nın bütün bilim iletişimi faaliyetlerini sürdürebilirdik. Bir düşünün: sadece %1'i...
O %1'i inşa etmemize yardım eder misiniz? Evrim Ağacı Premium üyesi olarak, ekibimizin size ve Türkiye'ye bilimi daha etkili ve profesyonel bir şekilde ulaştırmamızı mümkün kılmış olacaksınız. Ayrıca size olan minnetimizin bir ifadesi olarak, çok sayıda ayrıcalığa erişim sağlayacaksınız.
Makalelerimizin bilimsel gerçekleri doğru bir şekilde yansıtması için en üst düzey çabayı gösteriyoruz. Gözünüze doğru gelmeyen bir şey varsa, mümkünse güvenilir kaynaklarınızla birlikte bize ulaşın!
Bu makalemizle ilgili merak ettiğin bir şey mi var? Buraya tıklayarak sorabilirsin.
İlgili Sorular
Soru & Cevap Platformuna Git- 42
- 17
- 7
- 5
- 4
- 3
- 3
- 0
- 0
- 0
- 0
- 0
- A.V. Emeline. (2003). Abiogenesis And Photostimulated Heterogeneous Reactions In The Interstellar Medium And On Primitive Earth: Relevance To The Genesis Of Life. Journal of Photochemistry and Photobiology C: Photochemistry Reviews, sf: 203–224. | Arşiv Bağlantısı
- E. A. Kuzicheva, et al. (1999). The Possibility Of Nucleotide Abiogenic Synthesis In Conditions Of “Kosmos-2044” Satellite Space Flight. Advances in Space Research, sf: 393-396. doi: 10.1016/S0273-1177(99)00063-0. | Arşiv Bağlantısı
- M. D. Nussinov, et al. (1997). The Emergence Of The Non-Cellular Phase Of Life On The Fine-Grained Clayish Particles Of The Early Earth's Regolith. Biosystems, sf: 111-118. doi: 10.1016/S0303-2647(96)01699-1. | Arşiv Bağlantısı
- P. R. Bahn, et al. (1981). Models For Protocellular Photophosphorylation. Biosystems, sf: 3-14. doi: 10.1016/0303-2647(81)90017-4. | Arşiv Bağlantısı
- R. V. Solé. (2009). Evolution And Self-Assembly Of Protocells. The International Journal of Biochemistry & Cell Biology, sf: 274-284. doi: 10.1016/j.biocel.2008.10.004. | Arşiv Bağlantısı
- W. Ma, et al. (2010). The Emergence Of Ribozymes Synthesizing Membrane Components In Rna-Based Protocells. Biosystems, sf: 201-209. doi: 10.1016/j.biosystems.2009.11.003. | Arşiv Bağlantısı
- H. Schwegler, et al. (1986). The “Protocell”: A Mathematical Model Of Self-Maintenance. Biosystems, sf: 307-315. doi: 10.1016/0303-2647(86)90008-0. | Arşiv Bağlantısı
- J. Macía, et al. (2006). Protocell Self-Reproduction In A Spatially Extended Metabolism–Vesicle System. Elsevier BV, sf: 400-410. doi: 10.1016/j.jtbi.2006.10.021. | Arşiv Bağlantısı
- K. Tarumi, et al. (1987). A Nonlinear Treatment Of The Protocell Model By A Boundary Layer Approximation. Bulletin of Mathematical Biology, sf: 307-320. doi: 10.1007/BF02460122. | Arşiv Bağlantısı
- W. D. Snyder, et al. (1975). A Model For The Origin Of Stable Protocells In A Primitive Alkaline Ocean. Biosystems, sf: 222-229. doi: 10.1016/0303-2647(75)90029-5. | Arşiv Bağlantısı
- W. Stillwell. (1976). Facilitated Diffusion Of Amino Acids Across Bimolecular Lipid Membranes As A Model For Selective Accumulation Of Amino Acids In A Primordial Protocell. Biosystems, sf: 111-117. doi: 10.1016/0303-2647(76)90014-9. | Arşiv Bağlantısı
- S. W. Fox. (1980). The Origins Of Behavior In Macromolecules And Protocells. Comparative Biochemistry and Physiology Part B: Comparative Biochemistry, sf: 423-436. doi: 10.1016/0305-0491(80)90330-2. | Arşiv Bağlantısı
- E. Meléndez-Hevia, et al. (2007). From Prebiotic Chemistry To Cellular Metabolism—The Chemical Evolution Of Metabolism Before Darwinian Natural Selection. Elsevier BV, sf: 505-519. doi: 10.1016/j.jtbi.2007.11.012. | Arşiv Bağlantısı
- C. Fernando, et al. (2007). Natural Selection In Chemical Evolution. Journal of Theoretical Biology, sf: 152–167. | Arşiv Bağlantısı
- F. Kaneko, et al. (2005). Chemical Evolution Of Amino Acid Induced By Soft X-Ray With Synchrotron Radiation. Journal of Electron Spectroscopy and Related Phenomena, sf: 291–294. | Arşiv Bağlantısı
- K. Nakagawa, et al. (2009). Radiation-Induced Chemical Evolution Of Biomolecules. Radiation Physics and Chemistry, sf: 1198-1201. doi: 10.1016/j.radphyschem.2009.07.010. | Arşiv Bağlantısı
- A. Jäschke, et al. (2000). Evolution Of Dna And Rna As Catalysts For Chemical Reactions. Current Opinion in Chemical Biology, sf: 257-262. doi: 10.1016/S1367-5931(00)00086-7. | Arşiv Bağlantısı
- C. Giussani, et al. (2011). Anatomical Correlates For Category-Specific Naming Of Living And Non-Living Things. NeuroImage, sf: 323-329. doi: 10.1016/j.neuroimage.2011.01.080. | Arşiv Bağlantısı
- L. Witting. (2003). Major Life-History Transitions By Deterministic Directional Natural Selection. Journal of Theoretical Biology, sf: 389-406. doi: 10.1016/S0022-5193(03)00274-1. | Arşiv Bağlantısı
- M. Vaneechoutte, et al. (2009). From The Primordial Soup To The Latest Universal Common Ancestor. Research in Microbiology, sf: 437-440. doi: 10.1016/j.resmic.2009.09.002. | Arşiv Bağlantısı
- N. Lane. (2009). How Life Evolved: Forget The Primordial Soup. New Scientist, sf: 38-42. doi: 10.1016/S0262-4079(09)62756-1. | Arşiv Bağlantısı
- M. R. Edwards. (2002). From A Soup Or A Seed? Pyritic Metabolic Complexes In The Origin Of Life. Elsevier BV, sf: 178-181. doi: 10.1016/S0169-5347(97)01317-7. | Arşiv Bağlantısı
- D. L. Abel, et al. (2006). Self-Organization Vs. Self-Ordering Events In Life-Origin Models. Physics of Life Reviews, sf: 211-228. doi: 10.1016/j.plrev.2006.07.003. | Arşiv Bağlantısı
- S. Chooniedass-Kothari, et al. (2004). The Steroid Receptor Rna Activator Is The First Functional Rna Encoding A Protein. Wiley, sf: 43-47. doi: 10.1016/j.febslet.2004.03.104. | Arşiv Bağlantısı
- T. A. Steitz, et al. (2003). Rna, The First Macromolecular Catalyst: The Ribosome Is A Ribozyme. Elsevier BV, sf: 411-418. doi: 10.1016/S0968-0004(03)00169-5. | Arşiv Bağlantısı
- O. Lupi, et al. (2007). Did The First Virus Self-Assemble From Self-Replicating Prion Proteins And Rna?. Medical Hypotheses, sf: 724-730. doi: 10.1016/j.mehy.2007.03.031. | Arşiv Bağlantısı
- B. Ma, et al. (2008). Characters Of Very Ancient Proteins. Biochemical and Biophysical Research Communications, sf: 607-611. doi: 10.1016/j.bbrc.2007.12.014. | Arşiv Bağlantısı
- A. Vanerek, et al. (2006). Coacervate Complex Formation Between Cationic Polyacrylamide And Anionic Sulfonated Kraft Lignin. Colloids and Surfaces A: Physicochemical and Engineering Aspects, sf: 55–62. | Arşiv Bağlantısı
- R. J. Stewart, et al. (2011). Complex Coacervates As A Foundation For Synthetic Underwater Adhesives. Advances in Colloid and Interface Science, sf: 85-93. doi: 10.1016/j.cis.2010.10.009. | Arşiv Bağlantısı
- C. Sagan. (1975). Biogenesis, Abiogenesis, Biopoesis And All That. Origins of life, sf: 577-577. doi: 10.1007/BF00928906. | Arşiv Bağlantısı
- T. E. Pavlovskaya, et al. (1989). Conversion Of Light Energy Into Chemical One In Abiogenesis As A Precondition Of The Origin Of Life. Origins of life and evolution of the biosphere, sf: 227-228. doi: 10.1007/BF02388822. | Arşiv Bağlantısı
- N. Ono. (2005). Computational Studies On Conditions Of The Emergence Of Autopoietic Protocells. Biosystems, sf: 223-233. doi: 10.1016/j.biosystems.2005.04.005. | Arşiv Bağlantısı
- H. Zhang, et al. (2009). Bifurcation For A Free Boundary Problem Modeling A Protocell. Nonlinear Analysis: Theory, Methods & Applications, sf: 2779-2795. doi: 10.1016/j.na.2008.04.003. | Arşiv Bağlantısı
- S. W. Fox. (1983). Self-Organization Of The Protocell Was A Forward Process. Journal of Theoretical Biology, sf: 321-323. | Arşiv Bağlantısı
- R. Saladino, et al. (2012). Formamide In Non-Life/Life Transition. Physics of Life Reviews, sf: 121-123. doi: 10.1016/j.plrev.2012.01.006. | Arşiv Bağlantısı
- Y. N. Zhuravlev, et al. (2008). Modelling The Early Events Of Primordial Life. Ecological Modelling, sf: 536-544. doi: 10.1016/j.ecolmodel.2007.11.004. | Arşiv Bağlantısı
- B. Ma, et al. (2008). Characters Of Very Ancient Proteins. Biochemical and Biophysical Research Communications, sf: 607-611. doi: 10.1016/j.bbrc.2007.12.014. | Arşiv Bağlantısı
- H. Ohno, et al. (1991). Simple Coacervate Of Pullulan Formed By The Addition Of Poly(Ethylene Oxide) In An Aqueous Solution. Polymer, sf: 3062-3066. doi: 10.1016/0032-3861(91)90210-A. | Arşiv Bağlantısı
- H. Miyazaki, et al. (1996). Preparation Of Polyacrylamide Derivatives Showing Thermo-Reversible Coacervate Formation And Their Potential Application To Two-Phase Separation Processes. Polymer, sf: 681-685. doi: 10.1016/0032-3861(96)83156-9. | Arşiv Bağlantısı
- S. Tirard. (2014). Abiogenesis. Springer, Berlin, Heidelberg, sf: 1-1. doi: 10.1007/978-3-642-27833-4_2-4. | Arşiv Bağlantısı
- S. I. Walker, et al. (2017). Re-Conceptualizing The Origins Of Life. Philosophical Transactions of the Royal Society A: Mathematical, Physical and Engineering Sciences, sf: 20160337. doi: 10.1098/rsta.2016.0337. | Arşiv Bağlantısı
- G. Witzany. (2015). Crucial Steps To Life: From Chemical Reactions To Code Using Agents. Elsevier BV, sf: 49-57. doi: 10.1016/j.biosystems.2015.12.007. | Arşiv Bağlantısı
- E. N. . Trifonov. (2012). Vocabulary Of Definitions Of Life Suggests A Definition. Journal of Biomolecular Structure and Dynamics, sf: 259-266. doi: 10.1080/073911011010524992. | Arşiv Bağlantısı
- ScharfCaleb, et al. (2015). A Strategy For Origins Of Life Research. Astrobiology, sf: 1031-1042. doi: 10.1089/ast.2015.1113. | Arşiv Bağlantısı
- G. Horneck, et al. (2010). Space Microbiology. American Society for Microbiology, sf: 121-156. doi: 10.1128/MMBR.00016-09. | Arşiv Bağlantısı
- D. M. Balme. (1962). Development Of Biology In Aristotle And Theophrastus: Theory Of Spontaneous Generation. Phronesis, sf: 91-104. doi: 10.1163/156852862X00052. | Arşiv Bağlantısı
- C. Wickramasinghe. (2011). Bacterial Morphologies Supporting Cometary Panspermia: A Reappraisal. International Journal of Astrobiology, sf: 25-30. doi: 10.1017/S1473550410000157. | Arşiv Bağlantısı
- M. C. Weiss, et al. (2016). The Physiology And Habitat Of The Last Universal Common Ancestor. Nature Microbiology, sf: 1-8. doi: 10.1038/nmicrobiol.2016.116. | Arşiv Bağlantısı
- D. W. A. B. Weiss. (2005). Did Life Come From Another World?. Springer Science and Business Media LLC, sf: 64-71. doi: 10.1038/scientificamerican1105-64. | Arşiv Bağlantısı
- B. K. D. Pearce, et al. (2017). Origin Of The Rna World: The Fate Of Nucleobases In Warm Little Ponds. Proceedings of the National Academy of Sciences, sf: 11327-11332. doi: 10.1073/pnas.1710339114. | Arşiv Bağlantısı
- E. T. Parker, et al. (2011). Primordial Synthesis Of Amines And Amino Acids In A 1958 Miller H 2 S-Rich Spark Discharge Experiment. Proceedings of the National Academy of Sciences, sf: 5526-5531. doi: 10.1073/pnas.1019191108. | Arşiv Bağlantısı
- W. Martin, et al. (2003). On The Origins Of Cells: A Hypothesis For The Evolutionary Transitions From Abiotic Geochemistry To Chemoautotrophic Prokaryotes, And From Prokaryotes To Nucleated Cells. Philosophical Transactions of the Royal Society of London. Series B: Biological Sciences, sf: 59-85. doi: 10.1098/rstb.2002.1183. | Arşiv Bağlantısı
- H. J. Cleaves, et al. (2008). A Reassessment Of Prebiotic Organic Synthesis In Neutral Planetary Atmospheres. Origins of Life and Evolution of Biospheres, sf: 105-115. doi: 10.1007/s11084-007-9120-3. | Arşiv Bağlantısı
- J. D. Bernal. (1949). The Physical Basis Of Life. Proceedings of the Physical Society. Section A, sf: 537. doi: 10.1088/0370-1298/62/9/301. | Arşiv Bağlantısı
- K. Bahadur. (1975). Photochemical Formation Of Self-Sustaining Coacervates. Zentralblatt für Bakteriologie, Parasitenkunde, Infektionskrankheiten und Hygiene. Zweite Naturwissenschaftliche Abteilung: Allgemeine, Landwirtschaftliche und Technische Mikrobiologie, sf: 211-218. doi: 10.1016/S0044-4057(75)80076-1. | Arşiv Bağlantısı
- S. A. Wilde, et al. (2001). Evidence From Detrital Zircons For The Existence Of Continental Crust And Oceans On The Earth 4.4 Gyr Ago. Nature, sf: 175-178. doi: 10.1038/35051550. | Arşiv Bağlantısı
- J. L. Bada, et al. (2003). Prebiotic Soup--Revisiting The Miller Experiment. American Association for the Advancement of Science (AAAS), sf: 745-746. doi: 10.1126/science.1085145. | Arşiv Bağlantısı
- J. F. Kasting. (2006). Earth's Early Atmosphere. American Association for the Advancement of Science (AAAS), sf: 920-926. doi: 10.1126/science.11536547. | Arşiv Bağlantısı
- H. Follmann, et al. (2009). Darwin’s Warm Little Pond Revisited: From Molecules To The Origin Of Life. Naturwissenschaften, sf: 1265-1292. doi: 10.1007/s00114-009-0602-1. | Arşiv Bağlantısı
- R. Gomes, et al. (2005). Origin Of The Cataclysmic Late Heavy Bombardment Period Of The Terrestrial Planets. Nature, sf: 466-469. doi: 10.1038/nature03676. | Arşiv Bağlantısı
- T. Hassenkam, et al. (2017). Elements Of Eoarchean Life Trapped In Mineral Inclusions. Nature, sf: 78-81. doi: 10.1038/nature23261. | Arşiv Bağlantısı
- C. F. Chyba. (2005). Rethinking Earth's Early Atmosphere. American Association for the Advancement of Science (AAAS), sf: 962-963. doi: 10.1126/science.1113157. | Arşiv Bağlantısı
- K. A. Maher, et al. (1988). Impact Frustration Of The Origin Of Life. Nature, sf: 612-614. doi: 10.1038/331612a0. | Arşiv Bağlantısı
- J. W. Schopf, et al. (2017). Sims Analyses Of The Oldest Known Assemblage Of Microfossils Document Their Taxon-Correlated Carbon Isotope Compositions. Proceedings of the National Academy of Sciences, sf: 53-58. doi: 10.1073/pnas.1718063115. | Arşiv Bağlantısı
- A. Mann. (2018). Bashing Holes In The Tale Of Earth’s Troubled Youth. Springer Science and Business Media LLC, sf: 393-395. doi: 10.1038/d41586-018-01074-6. | Arşiv Bağlantısı
- S. L. Miller. (2006). A Production Of Amino Acids Under Possible Primitive Earth Conditions. American Association for the Advancement of Science (AAAS), sf: 528-529. doi: 10.1126/science.117.3046.528. | Arşiv Bağlantısı
- Y. Furukawa, et al. (2009). Biomolecule Formation By Oceanic Impacts On Early Earth. Nature Geoscience, sf: 62-66. doi: 10.1038/ngeo383. | Arşiv Bağlantısı
- P. Marigo, et al. (2020). Carbon Star Formation As Seen Through The Non-Monotonic Initial–Final Mass Relation. Nature Astronomy, sf: 1102-1110. doi: 10.1038/s41550-020-1132-1. | Arşiv Bağlantısı
- J. W. Schopf, et al. (2007). Evidence Of Archean Life: Stromatolites And Microfossils. Precambrian Research, sf: 141-155. doi: 10.1016/j.precamres.2007.04.009. | Arşiv Bağlantısı
- T. Djokic, et al. (2017). Earliest Signs Of Life On Land Preserved In Ca. 3.5 Ga Hot Spring Deposits. Nature Communications, sf: 1-9. doi: 10.1038/ncomms15263. | Arşiv Bağlantısı
- J. O'Donaghue. (2011). Oldest Fossils Show Early Life Was A Beach. New Scientist, sf: 13. doi: 10.1016/S0262-4079(11)62064-2. | Arşiv Bağlantısı
- J. W. Schopf. (2006). Fossil Evidence Of Archaean Life. Philosophical Transactions of the Royal Society B: Biological Sciences, sf: 869-885. doi: 10.1098/rstb.2006.1834. | Arşiv Bağlantısı
- Y. Ohtomo, et al. (2014). Evidence For Biogenic Graphite In Early Archaean Isua Metasedimentary Rocks. Nature Geoscience, sf: 25-28. doi: 10.1038/ngeo2025. | Arşiv Bağlantısı
- M. T. Rosing, et al. (2006). The Rise Of Continents—An Essay On The Geologic Consequences Of Photosynthesis. Palaeogeography, Palaeoclimatology, Palaeoecology, sf: 99-113. doi: 10.1016/j.palaeo.2006.01.007. | Arşiv Bağlantısı
- M. S. Dodd, et al. (2017). Evidence For Early Life In Earth’s Oldest Hydrothermal Vent Precipitates. Nature, sf: 60-64. doi: 10.1038/nature21377. | Arşiv Bağlantısı
- J. W. Morse, et al. (1998). Hadean Ocean Carbonate Geochemistry. Aquatic Geochemistry, sf: 301-319. doi: 10.1023/A:1009632230875. | Arşiv Bağlantısı
- C. Chyba, et al. (1992). Endogenous Production, Exogenous Delivery And Impact-Shock Synthesis Of Organic Molecules: An Inventory For The Origins Of Life. Nature, sf: 125-132. doi: 10.1038/355125a0. | Arşiv Bağlantısı
- NoffkeNora, et al. (2013). Microbially Induced Sedimentary Structures Recording An Ancient Ecosystem In The Ca. 3.48 Billion-Year-Old Dresser Formation, Pilbara, Western Australia. Astrobiology, sf: 1103-1124. doi: 10.1089/ast.2013.1030. | Arşiv Bağlantısı
- N. H. Sleep, et al. (2003). Annihilation Of Ecosystems By Large Asteroid Impacts On The Early Earth. Springer Science and Business Media LLC, sf: 139-142. doi: 10.1038/342139a0. | Arşiv Bağlantısı
- D. Wacey, et al. (2011). Microfossils Of Sulphur-Metabolizing Cells In 3.4-Billion-Year-Old Rocks Of Western Australia. Nature Geoscience, sf: 698-702. doi: 10.1038/ngeo1238. | Arşiv Bağlantısı
- R. J. Baumgartner, et al. (2019). Nano−Porous Pyrite And Organic Matter In 3.5-Billion-Year-Old Stromatolites Record Primordial Life. Geology, sf: 1039-1043. doi: 10.1130/G46365.1. | Arşiv Bağlantısı
- E. A. Bell, et al. (2015). Potentially Biogenic Carbon Preserved In A 4.1 Billion-Year-Old Zircon. Proceedings of the National Academy of Sciences, sf: 14518-14521. doi: 10.1073/pnas.1517557112. | Arşiv Bağlantısı
- T. R. Geballe, et al. (2011). Infrared Diffuse Interstellar Bands In The Galactic Centre Region. Nature, sf: 200-202. doi: 10.1038/nature10527. | Arşiv Bağlantısı
- N. Goldman, et al. (2013). Prebiotic Chemistry Within A Simple Impacting Icy Mixture. American Chemical Society (ACS), sf: 5124-5131. doi: 10.1021/jp402976n. | Arşiv Bağlantısı
- D. M. Hudgins, et al. (2005). Variations In The Peak Position Of The 6.2 Μm Interstellar Emission Feature: A Tracer Of N In The Interstellar Polycyclic Aromatic Hydrocarbon Population. The Astrophysical Journal, sf: 316. doi: 10.1086/432495. | Arşiv Bağlantısı
- W. R. Thompson, et al. (2008). Coloration And Darkening Of Methane Clathrate And Other Ices By Charged Particle Irradiation: Applications To The Outer Solar System. American Geophysical Union (AGU), sf: 14933-14947. doi: 10.1029/JA092iA13p14933. | Arşiv Bağlantısı
- D. A. García-Hernández, et al. (2010). Formation Of Fullerenes In H-Containing Planetary Nebulae. The Astrophysical Journal Letters, sf: L39. doi: 10.1088/2041-8205/724/1/L39. | Arşiv Bağlantısı
- Y. Oba, et al. (2022). Identifying The Wide Diversity Of Extraterrestrial Purine And Pyrimidine Nucleobases In Carbonaceous Meteorites. Nature Communications, sf: 1-10. doi: 10.1038/s41467-022-29612-x. | Arşiv Bağlantısı
- P. Ehrenfreund, et al. (2010). Cosmic Carbon Chemistry: From The Interstellar Medium To The Early Earth. Cold Spring Harbor Perspectives in Biology, sf: a002097. doi: 10.1101/cshperspect.a002097. | Arşiv Bağlantısı
- V. V. Goncharuk, et al. (2015). Water And Carbon Dioxide As The Main Precursors Of Organic Matter On Earth And In Space. Journal of Water Chemistry and Technology, sf: 2-3. doi: 10.3103/S1063455X15010026. | Arşiv Bağlantısı
- M. S. Gudipati, et al. (2012). In-Situ Probing Of Radiation-Induced Processing Of Organics In Astrophysical Ice Analogs—Novel Laser Desorption Laser Ionization Time-Of-Flight Mass Spectroscopic Studies. The Astrophysical Journal Letters, sf: L24. doi: 10.1088/2041-8205/756/1/L24. | Arşiv Bağlantısı
- M. D’Ischia, et al. (2019). Astrochemistry And Astrobiology: Materials Science In Wonderland?. International Journal of Molecular Sciences, sf: 4079. doi: 10.3390/ijms20174079. | Arşiv Bağlantısı
- Z. Martins, et al. (2008). Extraterrestrial Nucleobases In The Murchison Meteorite. Earth and Planetary Science Letters, sf: 130-136. doi: 10.1016/j.epsl.2008.03.026. | Arşiv Bağlantısı
- Z. Martins. (2011). Organic Chemistry Of Carbonaceous Meteorites. Elements, sf: 35-40. doi: 10.2113/gselements.7.1.35. | Arşiv Bağlantısı
- E. Gallori. (2011). Astrochemistry And The Origin Of Genetic Material. Rendiconti Lincei, sf: 113-118. doi: 10.1007/s12210-011-0118-4. | Arşiv Bağlantısı
- M. P. Callahan, et al. (2011). Carbonaceous Meteorites Contain A Wide Range Of Extraterrestrial Nucleobases. Proceedings of the National Academy of Sciences, sf: 13995-13998. doi: 10.1073/pnas.1106493108. | Arşiv Bağlantısı
- S. Kwok, et al. (2011). Mixed Aromatic–Aliphatic Organic Nanoparticles As Carriers Of Unidentified Infrared Emission Features. Nature, sf: 80-83. doi: 10.1038/nature10542. | Arşiv Bağlantısı
- J. K. Jørgensen, et al. (2012). Detection Of The Simplest Sugar, Glycolaldehyde, In A Solar-Type Protostar With Alma. The Astrophysical Journal Letters, sf: L4. doi: 10.1088/2041-8205/757/1/L4. | Arşiv Bağlantısı
- H. J. C. II. (2010). The Origin Of The Biologically Coded Amino Acids. Journal of Theoretical Biology, sf: 490-498. doi: 10.1016/j.jtbi.2009.12.014. | Arşiv Bağlantısı
- Y. Furukawa, et al. (2019). Extraterrestrial Ribose And Other Sugars In Primitive Meteorites. Proceedings of the National Academy of Sciences, sf: 24440-24445. doi: 10.1073/pnas.1907169116. | Arşiv Bağlantısı
- I. A. Chen. (2006). The Emergence Of Cells During The Origin Of Life. American Association for the Advancement of Science (AAAS), sf: 1558-1559. doi: 10.1126/science.1137541. | Arşiv Bağlantısı
- C. Menor-Salván, et al. (2009). Synthesis Of Pyrimidines And Triazines In Ice: Implications For The Prebiotic Chemistry Of Nucleobases. Wiley, sf: 4411-4418. doi: 10.1002/chem.200802656. | Arşiv Bağlantısı
- J. ORÓ. (1961). Mechanism Of Synthesis Of Adenine From Hydrogen Cyanide Under Possible Primitive Earth Conditions. Nature, sf: 1193-1194. doi: 10.1038/1911193a0. | Arşiv Bağlantısı
- L. E. Orgel. (2004). Prebiotic Adenine Revisited: Eutectics And Photochemistry. Origins of life and evolution of the biosphere, sf: 361-369. doi: 10.1023/B:ORIG.0000029882.52156.c2. | Arşiv Bağlantısı
- I. A. Chen, et al. (2010). From Self-Assembled Vesicles To Protocells. Cold Spring Harbor Perspectives in Biology, sf: a002170. doi: 10.1101/cshperspect.a002170. | Arşiv Bağlantısı
- M. Eigen, et al. (1978). The Hypercycle. The Science of Nature, sf: 341-369. doi: 10.1007/BF00439699. | Arşiv Bağlantısı
- M. Ferus, et al. (2014). High-Energy Chemistry Of Formamide: A Unified Mechanism Of Nucleobase Formation. Proceedings of the National Academy of Sciences, sf: 657-662. doi: 10.1073/pnas.1412072111. | Arşiv Bağlantısı
- J. Oró, et al. (1962). Synthesis Of Purines Under Possible Primitive Earth Conditions: Ii. Purine Intermediates From Hydrogen Cyanide. Archives of Biochemistry and Biophysics, sf: 293-313. doi: 10.1016/0003-9861(62)90412-5. | Arşiv Bağlantısı
- M. Eigen, et al. (1978). The Hypercycle. Naturwissenschaften, sf: 7-41. doi: 10.1007/BF00420631. | Arşiv Bağlantısı
- D. Roy, et al. (2007). Chemical Evolution: The Mechanism Of The Formation Of Adenine Under Prebiotic Conditions. Proceedings of the National Academy of Sciences, sf: 17272-17277. doi: 10.1073/pnas.0708434104. | Arşiv Bağlantısı
- M. P. Robertson, et al. (1995). An Efficient Prebiotic Synthesis Of Cytosine And Uracil. Nature, sf: 772-774. doi: 10.1038/375772a0. | Arşiv Bağlantısı
- D. Segré, et al. (2001). The Lipid World. Origins of life and evolution of the biosphere, sf: 119-145. doi: 10.1023/A:1006746807104. | Arşiv Bağlantısı
- M. Levy, et al. (2000). Prebiotic Synthesis Of Adenine And Amino Acids Under Europa-Like Conditions. Icarus, sf: 609-613. doi: 10.1006/icar.2000.6365. | Arşiv Bağlantısı
- B. Basile, et al. (1984). Prebiotic Syntheses Of Purines And Pyrimidines. Advances in Space Research, sf: 125-131. doi: 10.1016/0273-1177(84)90554-4. | Arşiv Bağlantısı
- M. Tessera. (2011). Origin Of Evolution Versus Origin Of Life: A Shift Of Paradigm. International Journal of Molecular Sciences, sf: 3445-3458. doi: 10.3390/ijms12063445. | Arşiv Bağlantısı
- M. Eigen, et al. (1977). A Principle Of Natural Self-Organization. Naturwissenschaften, sf: 541-565. doi: 10.1007/BF00450633. | Arşiv Bağlantısı
- R. Saladino, et al. (2012). From The One-Carbon Amide Formamide To Rna All The Steps Are Prebiotically Possible. Biochimie, sf: 1451-1456. doi: 10.1016/j.biochi.2012.02.018. | Arşiv Bağlantısı
- R. Saladino, et al. (2012). Formamide And The Origin Of Life. Physics of Life Reviews, sf: 84-104. doi: 10.1016/j.plrev.2011.12.002. | Arşiv Bağlantısı
- R. Breslow. (1959). On The Mechanism Of The Formose Reaction. Tetrahedron Letters, sf: 22-26. doi: 10.1016/S0040-4039(01)99487-0. | Arşiv Bağlantısı
- R. Shapiro. (2007). A Simpler Origin For Life. Springer Science and Business Media LLC, sf: 46-53. doi: 10.1038/scientificamerican0607-46. | Arşiv Bağlantısı
- O. Markovitch, et al. (2012). Excess Mutual Catalysis Is Required For Effective Evolvability. Artificial Life, sf: 243-266. doi: 10.1162/ARTL_a_00064. | Arşiv Bağlantısı
- S. A. Benner, et al. (2019). When Did Life Likely Emerge On Earth In An Rna‐First Process?. Wiley. doi: 10.1002/syst.201900035. | Arşiv Bağlantısı
- W. Junge, et al. (2015). Atp Synthase. Annual Reviews, sf: 631-657. doi: 10.1146/annurev-biochem-060614-034124. | Arşiv Bağlantısı
- T. R. Cech. (2012). The Rna Worlds In Context. Cold Spring Harbor Perspectives in Biology, sf: a006742. doi: 10.1101/cshperspect.a006742. | Arşiv Bağlantısı
- M. P. Robertson, et al. (2012). The Origins Of The Rna World. Cold Spring Harbor Perspectives in Biology, sf: a003608. doi: 10.1101/cshperspect.a003608. | Arşiv Bağlantısı
- L. E. Orgel. (2003). Some Consequences Of The Rna World Hypothesis. Origins of life and evolution of the biosphere, sf: 211-218. doi: 10.1023/A:1024616317965. | Arşiv Bağlantısı
- A. W. J. Muller, et al. (2006). Thermal Energy And The Origin Of Life. Origins of Life and Evolution of Biospheres, sf: 177-189. doi: 10.1007/s11084-005-9003-4. | Arşiv Bağlantısı
- M. Yarus. (2011). Getting Past The Rna World: The Initial Darwinian Ancestor. Cold Spring Harbor Perspectives in Biology, sf: a003590. doi: 10.1101/cshperspect.a003590. | Arşiv Bağlantısı
- A. W. J. Muller. (1995). Were The First Organisms Heat Engines? A New Model For Biogenesis And The Early Evolution Of Biological Energy Conversion. Progress in Biophysics and Molecular Biology, sf: 193-231. doi: 10.1016/0079-6107(95)00004-7. | Arşiv Bağlantısı
- S. D. Copley, et al. (2007). The Origin Of The Rna World: Co-Evolution Of Genes And Metabolism. Elsevier BV, sf: 430-443. doi: 10.1016/j.bioorg.2007.08.001. | Arşiv Bağlantısı
- T. A. Lincoln, et al. (2009). Self-Sustained Replication Of An Rna Enzyme. American Association for the Advancement of Science (AAAS), sf: 1229-1232. doi: 10.1126/science.1167856. | Arşiv Bağlantısı
- W. Gilbert. (1986). Origin Of Life: The Rna World. Nature, sf: 618-618. doi: 10.1038/319618a0. | Arşiv Bağlantısı
- G. F. Joyce. (2009). Evolution In An Rna World. Cold Spring Harbor Symposia on Quantitative Biology, sf: 17-23. doi: 10.1101/sqb.2009.74.004. | Arşiv Bağlantısı
- G. E. Fox. (2010). Origin And Evolution Of The Ribosome. Cold Spring Harbor Perspectives in Biology, sf: a003483. doi: 10.1101/cshperspect.a003483. | Arşiv Bağlantısı
- M. Neveu, et al. (2013). The “Strong” Rna World Hypothesis: Fifty Years Old. Mary Ann Liebert Inc, sf: 391-403. doi: 10.1089/ast.2012.0868. | Arşiv Bağlantısı
- A. V. Vlassov, et al. (2005). The Rna World On Ice: A New Scenario For The Emergence Of Rna Information. Journal of Molecular Evolution, sf: 264-273. doi: 10.1007/s00239-004-0362-7. | Arşiv Bağlantısı
- E. V. Koonin. (2007). The Cosmological Model Of Eternal Inflation And The Transition From Chance To Biological Evolution In The History Of Life. Biology Direct, sf: 1-21. doi: 10.1186/1745-6150-2-15. | Arşiv Bağlantısı
- G. W. Hoffmann. (2003). The Stochastic Theory Of The Origin Of The Genetic Code. Annual Reviews, sf: 123-144. doi: 10.1146/annurev.pc.26.100175.001011. | Arşiv Bağlantısı
- H. Bernstein, et al. (2015). The Darwinian Dynamic. The Quarterly Review of Biology, sf: 185-207. doi: 10.1086/413216. | Arşiv Bağlantısı
- M. D. Nussinov, et al. (1997). The Emergence Of The Non-Cellular Phase Of Life On The Fine-Grained Clayish Particles Of The Early Earth's Regolith. Biosystems, sf: 111-118. doi: 10.1016/S0303-2647(96)01699-1. | Arşiv Bağlantısı
- C. R. Woese, et al. (2006). Phylogenetic Structure Of The Prokaryotic Domain: The Primary Kingdoms. Proceedings of the National Academy of Sciences, sf: 5088-5090. doi: 10.1073/pnas.74.11.5088. | Arşiv Bağlantısı
- A. Kühnlein, et al. (2021). Trna Sequences Can Assemble Into A Replicator. eLife Sciences Publications, Ltd. doi: 10.7554/eLife.63431. | Arşiv Bağlantısı
- W. Martin, et al. (2003). On The Origins Of Cells: A Hypothesis For The Evolutionary Transitions From Abiotic Geochemistry To Chemoautotrophic Prokaryotes, And From Prokaryotes To Nucleated Cells. Philosophical Transactions of the Royal Society of London. Series B: Biological Sciences, sf: 59-85. doi: 10.1098/rstb.2002.1183. | Arşiv Bağlantısı
- A. Roldan, et al. (2015). Bio-Inspired Co2 Conversion By Iron Sulfide Catalysts Under Sustainable Conditions. Chemical Communications, sf: 7501-7504. doi: 10.1039/C5CC02078F. | Arşiv Bağlantısı
- J. A. Baross, et al. (1985). Submarine Hydrothermal Vents And Associated Gradient Environments As Sites For The Origin And Evolution Of Life. Origins of life and evolution of the biosphere, sf: 327-345. doi: 10.1007/BF01808177. | Arşiv Bağlantısı
- H. F. Noller. (2012). Evolution Of Protein Synthesis From An Rna World. Cold Spring Harbor Perspectives in Biology, sf: a003681. doi: 10.1101/cshperspect.a003681. | Arşiv Bağlantısı
- G. W. Hoffmann. (1974). On The Origin Of The Genetic Code And The Stability Of The Translation Apparatus. Journal of Molecular Biology, sf: 349-362. doi: 10.1016/0022-2836(74)90024-2. | Arşiv Bağlantısı
- E. L. Shock, et al. (2015). Principles Of Geobiochemistry. Elements, sf: 395-401. doi: 10.2113/gselements.11.6.395. | Arşiv Bağlantısı
- J. P. Amend, et al. (2013). The Energetics Of Organic Synthesis Inside And Outside The Cell. Philosophical Transactions of the Royal Society B: Biological Sciences, sf: 20120255. doi: 10.1098/rstb.2012.0255. | Arşiv Bağlantısı
- M. J. RUSSELL, et al. (1997). The Emergence Of Life From Iron Monosulphide Bubbles At A Submarine Hydrothermal Redox And Ph Front. Journal of the Geological Society, sf: 377-402. doi: 10.1144/gsjgs.154.3.0377. | Arşiv Bağlantısı
- Nature. (2016). Early Life Liked It Hot. Nature, sf: 468-468. doi: 10.1038/535468b. | Arşiv Bağlantısı
- T. Cavalier-Smith. (2006). Rooting The Tree Of Life By Transition Analyses. Biology Direct, sf: 1-83. doi: 10.1186/1745-6150-1-19. | Arşiv Bağlantısı
- L. E. Orgel. (2006). The Maintenance Of The Accuracy Of Protein Synthesis And Its Relevance To Ageing. Proceedings of the National Academy of Sciences, sf: 517-521. doi: 10.1073/pnas.49.4.517. | Arşiv Bağlantısı
- R. E. Valas, et al. (2011). The Origin Of A Derived Superkingdom: How A Gram-Positive Bacterium Crossed The Desert To Become An Archaeon. Biology Direct, sf: 1-33. doi: 10.1186/1745-6150-6-16. | Arşiv Bağlantısı
- L. E. Orgel. (1994). The Origin Of Life On The Earth. Springer Science and Business Media LLC, sf: 76-83. doi: 10.1038/scientificamerican1094-76. | Arşiv Bağlantısı
- M. Colín-García. (2017). Hydrothermal Vents And Prebiotic Chemistry: A Review. Sociedad Geologica Mexicana, sf: 599-620. doi: 10.18268/BSGM2016v68n3a13. | Arşiv Bağlantısı
- W. Martin, et al. (2006). On The Origin Of Biochemistry At An Alkaline Hydrothermal Vent. The Royal Society, sf: 1887-1926. doi: 10.1098/rstb.2006.1881. | Arşiv Bağlantısı
- J. G. Forsythe, et al. (2015). Ester‐Mediated Amide Bond Formation Driven By Wet–Dry Cycles: A Possible Path To Polypeptides On The Prebiotic Earth. Wiley, sf: 9871-9875. doi: 10.1002/anie.201503792. | Arşiv Bağlantısı
- A. Y. Mulkidjanian, et al. (2012). Origin Of First Cells At Terrestrial, Anoxic Geothermal Fields. Proceedings of the National Academy of Sciences. doi: 10.1073/pnas.1117774109. | Arşiv Bağlantısı
- W. Huang, et al. (2006). One-Step, Regioselective Synthesis Of Up To 50-Mers Of Rna Oligomers By Montmorillonite Catalysis. American Chemical Society (ACS), sf: 8914-8919. doi: 10.1021/ja061782k. | Arşiv Bağlantısı
- A. B. Subramaniam, et al. (2011). Semi-Permeable Vesicles Composed Of Natural Clay. Soft Matter, sf: 2600-2612. doi: 10.1039/C0SM01354D. | Arşiv Bağlantısı
- K. R. POPPER. (1990). Pyrite And The Origin Of Life. Nature, sf: 387-387. doi: 10.1038/344387a0. | Arşiv Bağlantısı
- Y. Vallee, et al. (2017). At The Very Beginning Of Life On Earth: The Thiol-Rich Peptide (Trp) World Hypothesis. International Journal of Developmental Biology, sf: 471-478. doi: 10.1387/ijdb.170028yv. | Arşiv Bağlantısı
- K. Adamala, et al. (2013). Nonenzymatic Template-Directed Rna Synthesis Inside Model Protocells. American Association for the Advancement of Science (AAAS), sf: 1098-1100. doi: 10.1126/science.1241888. | Arşiv Bağlantısı
- B. Damer, et al. (2020). The Hot Spring Hypothesis For An Origin Of Life. Astrobiology, sf: 429-452. doi: 10.1089/ast.2019.2045. | Arşiv Bağlantısı
- H. Hartman. (1998). Photosynthesis And The Origin Of Life. Origins of life and evolution of the biosphere, sf: 515-521. doi: 10.1023/A:1006548904157. | Arşiv Bağlantısı
- J. L. England. (2013). Statistical Physics Of Self-Replication. AIP Publishing, sf: 121923. doi: 10.1063/1.4818538. | Arşiv Bağlantısı
- K. Chandru, et al. (2016). The Abiotic Chemistry Of Thiolated Acetate Derivatives And The Origin Of Life. Scientific Reports, sf: 1-11. doi: 10.1038/srep29883. | Arşiv Bağlantısı
- M. A. Keller, et al. (2014). Non‐Enzymatic Glycolysis And Pentose Phosphate Pathway‐Like Reactions In A Plausiblearchean Ocean. EMBO, sf: 725. doi: 10.1002/msb.20145228. | Arşiv Bağlantısı
- A. Y. Mulkidjanian. (2009). On The Origin Of Life In The Zinc World: 1. Photosynthesizing, Porous Edifices Built Of Hydrothermally Precipitated Zinc Sulfide As Cradles Of Life On Earth. Biology Direct, sf: 1-39. doi: 10.1186/1745-6150-4-26. | Arşiv Bağlantısı
- G. Wächtershäuser. (2020). Before Enzymes And Templates: Theory Of Surface Metabolism.. American Society for Microbiology, sf: 452-484. doi: 10.1128/MMBR.52.4.452-484.1988. | Arşiv Bağlantısı
- L. E. Orgel. (2002). Self-Organizing Biochemical Cycles. Proceedings of the National Academy of Sciences, sf: 12503-12507. doi: 10.1073/pnas.220406697. | Arşiv Bağlantısı
- K. Chandru, et al. (2018). Simple Prebiotic Synthesis Of High Diversity Dynamic Combinatorial Polyester Libraries. Communications Chemistry, sf: 1-8. doi: 10.1038/s42004-018-0031-1. | Arşiv Bağlantısı
- A. B. Macallum. (1926). The Paleochemistry Of The Body Fluids And Tissues. Physiological Reviews, sf: 316-357. doi: 10.1152/physrev.1926.6.2.316. | Arşiv Bağlantısı
- A. Y. Mulkidjanian, et al. (2009). On The Origin Of Life In The Zinc World. 2. Validation Of The Hypothesis On The Photosynthesizing Zinc Sulfide Edifices As Cradles Of Life On Earth. Biology Direct, sf: 1-37. doi: 10.1186/1745-6150-4-27. | Arşiv Bağlantısı
- R. F. Fox. (2009). Review Of Stuart Kauffman, The Origins Of Order: Self-Organization And Selection In Evolution. Elsevier BV, sf: 2698-2699. doi: 10.1016/s0006-3495(93)81321-3. | Arşiv Bağlantısı
- C. Huber, et al. (2002). Peptides By Activation Of Amino Acids With Co On (Ni,Fe)S Surfaces: Implications For The Origin Of Life. American Association for the Advancement of Science (AAAS), sf: 670-672. doi: 10.1126/science.281.5377.670. | Arşiv Bağlantısı
- R. Plasson, et al. (2007). Emergence Of Homochirality In Far-From-Equilibrium Systems: Mechanisms And Role In Prebiotic Chemistry. Wiley, sf: 589-600. doi: 10.1002/chir.20440. | Arşiv Bağlantısı
- A. Y. Mulkidjanian, et al. (2012). Origin Of First Cells At Terrestrial, Anoxic Geothermal Fields. Proceedings of the National Academy of Sciences. doi: 10.1073/pnas.1117774109. | Arşiv Bağlantısı
- F. Jafarpour, et al. (2015). Noise-Induced Mechanism For Biological Homochirality Of Early Life Self-Replicators. Physical Review Letters, sf: 158101. doi: 10.1103/PhysRevLett.115.158101. | Arşiv Bağlantısı
- F. Jafarpour, et al. (2017). Noise-Induced Symmetry Breaking Far From Equilibrium And The Emergence Of Biological Homochirality. Physical Review E, sf: 032407. doi: 10.1103/PhysRevE.95.032407. | Arşiv Bağlantısı
- C. Davidovich, et al. (2009). The Evolving Ribosome: From Non-Coded Peptide Bond Formation To Sophisticated Translation Machinery. Research in Microbiology, sf: 487-492. doi: 10.1016/j.resmic.2009.07.004. | Arşiv Bağlantısı
- K. Soai, et al. (2002). Asymmetric Autocatalysis And The Origin Of Chiral Homogeneity In Organic Compounds. Wiley, sf: 321-332. doi: 10.1002/tcr.1017. | Arşiv Bağlantısı
- F. C. Frank. (1953). On Spontaneous Asymmetric Synthesis. Biochimica et Biophysica Acta, sf: 459-463. doi: 10.1016/0006-3002(53)90082-1. | Arşiv Bağlantısı
- T. Shibata, et al. (2002). Highly Enantioselective Catalytic Asymmetric Automultiplication Of Chiral Pyrimidyl Alcohol. American Chemical Society (ACS), sf: 471-472. doi: 10.1021/ja953066g. | Arşiv Bağlantısı
- S. Clark. (2003). Polarized Starlight And The Handedness Of Life. Sigma Xi, sf: 336. doi: 10.1511/1999.4.336. | Arşiv Bağlantısı
- J. F. Atkins, et al. (2002). The 22Nd Amino Acid. American Association for the Advancement of Science (AAAS), sf: 1409-1410. doi: 10.1126/science.1073339. | Arşiv Bağlantısı
- Y. Zhou, et al. (2021). A Widespread Pathway For Substitution Of Adenine By Diaminopurine In Phage Genomes. American Association for the Advancement of Science (AAAS), sf: 512-516. doi: 10.1126/science.abe4882. | Arşiv Bağlantısı
- D. Sleiman, et al. (2021). A Third Purine Biosynthetic Pathway Encoded By Aminoadenine-Based Viral Dna Genomes. American Association for the Advancement of Science (AAAS), sf: 516-520. doi: 10.1126/science.abe6494. | Arşiv Bağlantısı
- M. W. Grome, et al. (2021). Ztcg: Viruses Expand The Genetic Alphabet. American Association for the Advancement of Science (AAAS), sf: 460-461. doi: 10.1126/science.abh3571. | Arşiv Bağlantısı
- V. Pezo, et al. (2021). Noncanonical Dna Polymerization By Aminoadenine-Based Siphoviruses. American Association for the Advancement of Science (AAAS), sf: 520-524. doi: 10.1126/science.abe6542. | Arşiv Bağlantısı
- C. Alff-Steinberger. (2006). The Genetic Code And Error Transmission. Proceedings of the National Academy of Sciences, sf: 584-591. doi: 10.1073/pnas.64.2.584. | Arşiv Bağlantısı
- C. Mayer-Bacon, et al. (2021). Evolution As A Guide To Designing Xeno Amino Acid Alphabets. International Journal of Molecular Sciences, sf: 2787. doi: 10.3390/ijms22062787. | Arşiv Bağlantısı
- A. Eschenmoser. (2002). Chemical Etiology Of Nucleic Acid Structure. American Association for the Advancement of Science (AAAS), sf: 2118-2124. doi: 10.1126/science.284.5423.2118. | Arşiv Bağlantısı
- S. Hoshika, et al. (2019). Hachimoji Dna And Rna: A Genetic System With Eight Building Blocks. American Association for the Advancement of Science (AAAS), sf: 884-887. doi: 10.1126/science.aat0971. | Arşiv Bağlantısı
- F. CRICK. (1970). Central Dogma Of Molecular Biology. Nature, sf: 561-563. doi: 10.1038/227561a0. | Arşiv Bağlantısı
- I. Nikić‐Spiegel. (2020). Expanding The Genetic Code For Neuronal Studies. Wiley, sf: 3169-3179. doi: 10.1002/cbic.202000300. | Arşiv Bağlantısı
- A. Dumas, et al. (2014). Designing Logical Codon Reassignment – Expanding The Chemistry In Biology. Chemical Science, sf: 50-69. doi: 10.1039/C4SC01534G. | Arşiv Bağlantısı
- C. C. Liu, et al. (2010). Adding New Chemistries To The Genetic Code. Annual Reviews, sf: 413-444. doi: 10.1146/annurev.biochem.052308.105824. | Arşiv Bağlantısı
- A. Ambrogelly, et al. (2007). Natural Expansion Of The Genetic Code. Nature Chemical Biology, sf: 29-35. doi: 10.1038/nchembio847. | Arşiv Bağlantısı
- A. X. Zhou, et al. (2019). Progress Toward Eukaryotic Semisynthetic Organisms: Translation Of Unnatural Codons. American Chemical Society (ACS), sf: 20166-20170. doi: 10.1021/jacs.9b09080. | Arşiv Bağlantısı
- Proceedings of the Royal Society of London. Series B: Biological Sciences. (1991). Four Letters In The Genetic Alphabet: A Frozen Evolutionary Optimum?. Proceedings of the Royal Society of London. Series B: Biological Sciences, sf: 91-99. doi: 10.1098/rspb.1991.0093. | Arşiv Bağlantısı
- A. L. Weber, et al. (1981). Reasons For The Occurrence Of The Twenty Coded Protein Amino Acids. Journal of Molecular Evolution, sf: 273-284. doi: 10.1007/BF01795749. | Arşiv Bağlantısı
- E. N. Trifonov. (2000). Consensus Temporal Order Of Amino Acids And Evolution Of The Triplet Code. Gene, sf: 139-151. doi: 10.1016/S0378-1119(00)00476-5. | Arşiv Bağlantısı
- R. Geyer, et al. (2018). On The Efficiency Of The Genetic Code After Frameshift Mutations. PeerJ, sf: e4825. doi: 10.7717/peerj.4825. | Arşiv Bağlantısı
- P. P. Gardner, et al. (2003). Optimal Alphabets For An Rna World. Proceedings of the Royal Society of London. Series B: Biological Sciences, sf: 1177-1182. doi: 10.1098/rspb.2003.2355. | Arşiv Bağlantısı
- A. R. Nödling, et al. (2019). Using Genetically Incorporated Unnatural Amino Acids To Control Protein Functions In Mammalian Cells. Essays in Biochemistry, sf: 237-266. doi: 10.1042/EBC20180042. | Arşiv Bağlantısı
- P. G. Higgs, et al. (2009). A Thermodynamic Basis For Prebiotic Amino Acid Synthesis And The Nature Of The First Genetic Code. Mary Ann Liebert Inc, sf: 483-490. doi: 10.1089/ast.2008.0280. | Arşiv Bağlantısı
- S. J. Freeland, et al. (2002). Do Proteins Predate Dna?. American Association for the Advancement of Science (AAAS), sf: 690-692. doi: 10.1126/science.286.5440.690. | Arşiv Bağlantısı
- G. P. Fournier, et al. (2015). Ancestral Reconstruction Of A Pre-Luca Aminoacyl-Trna Synthetase Ancestor Supports The Late Addition Of Trp To The Genetic Code. Journal of Molecular Evolution, sf: 171-185. doi: 10.1007/s00239-015-9672-1. | Arşiv Bağlantısı
- H. Štorchová. (1994). Gesteland, R.f., Atkins, J.f. (Ed.): The Rna World. Biologia plantarum, sf: 358-358. doi: 10.1007/BF02920931. | Arşiv Bağlantısı
- V. Tretyachenko, et al. (2021). Unevolved Proteins From Modern And Prebiotic Amino Acids Manifest Distinct Structural Profiles. bioRxiv, sf: 2021.08.29.458031. doi: 10.1101/2021.08.29.458031. | Arşiv Bağlantısı
- G. F. Joyce. (2002). The Antiquity Of Rna-Based Evolution. Nature, sf: 214-221. doi: 10.1038/418214a. | Arşiv Bağlantısı
- J. C. Xavier, et al. (2020). Autocatalytic Chemical Networks At The Origin Of Metabolism. Proceedings of the Royal Society B, sf: 20192377. doi: 10.1098/rspb.2019.2377. | Arşiv Bağlantısı
- I. Prigogine, et al. (2008). Thermodynamics Of Evolution. AIP Publishing, sf: 23-28. doi: 10.1063/1.3071090. | Arşiv Bağlantısı
- R. Krishnamurthy. (2018). Life's Biological Chemistry: A Destiny Or Destination Starting From Prebiotic Chemistry?. Wiley, sf: 16708-16715. doi: 10.1002/chem.201801847. | Arşiv Bağlantısı
- J. M. Horowitz, et al. (2017). Spontaneous Fine-Tuning To Environment In Many-Species Chemical Reaction Networks. Proceedings of the National Academy of Sciences, sf: 7565-7570. doi: 10.1073/pnas.1700617114. | Arşiv Bağlantısı
- N. V. Hud. (2018). Searching For Lost Nucleotides Of The Pre-Rna World With A Self-Refining Model Of Early Earth. Nature Communications, sf: 1-4. doi: 10.1038/s41467-018-07389-2. | Arşiv Bağlantısı
- V. Vasas, et al. (2010). Lack Of Evolvability In Self-Sustaining Autocatalytic Networks Constraints Metabolism-First Scenarios For The Origin Of Life. Proceedings of the National Academy of Sciences, sf: 1470-1475. doi: 10.1073/pnas.0912628107. | Arşiv Bağlantısı
- B. A. Anderson, et al. (2020). The Unexpected Base‐Pairing Behavior Of Cyanuric Acid In Rna And Ribose Versus Cyanuric Acid Induced Helicene Assembly Of Nucleic Acids: Implications For The Pre‐Rna Paradigm. Wiley, sf: 4033-4042. doi: 10.1002/chem.202004397. | Arşiv Bağlantısı
- C. Anastasi, et al. (2007). Rna: Prebiotic Product, Or Biotic Invention?. Wiley, sf: 721-739. doi: 10.1002/cbdv.200790060. | Arşiv Bağlantısı
- A. Lazcano, et al. (2004). The Origin And Early Evolution Of Life: Prebiotic Chemistry, The Pre-Rna World, And Time. Elsevier BV, sf: 793-798. doi: 10.1016/s0092-8674(00)81263-5. | Arşiv Bağlantısı
- W. Hordijk, et al. (2017). Chasing The Tail: The Emergence Of Autocatalytic Networks. Biosystems, sf: 1-10. doi: 10.1016/j.biosystems.2016.12.002. | Arşiv Bağlantısı
- B. . SHENHAV, et al. (2011). Mesobiotic Emergence: Molecular And Ensemble Complexity In Early Evolution. Advances in Complex Systems, sf: 15-35. doi: 10.1142/S0219525903000785. | Arşiv Bağlantısı
- S. D. Fried, et al. (2022). Peptides Before And During The Nucleotide World: An Origins Story Emphasizing Cooperation Between Proteins And Nucleic Acids. Journal of the Royal Society Interface. doi: 10.1098/rsif.2021.0641. | Arşiv Bağlantısı
- Z. Peng, et al. (2020). An Ecological Framework For The Analysis Of Prebiotic Chemical Reaction Networks. Journal of Theoretical Biology, sf: 110451. doi: 10.1016/j.jtbi.2020.110451. | Arşiv Bağlantısı
- P. Chvykov, et al. (2020). Low Rattling: A Predictive Principle For Self-Organization In Active Collectives. American Association for the Advancement of Science (AAAS), sf: 90-95. doi: 10.1126/science.abc6182. | Arşiv Bağlantısı
- A. Murugan, et al. (2015). Undesired Usage And The Robust Self-Assembly Of Heterogeneous Structures. Nature Communications, sf: 1-10. doi: 10.1038/ncomms7203. | Arşiv Bağlantısı
- K. Michaelian. (2011). Thermodynamic Dissipation Theory For The Origin Of Life. Earth System Dynamics, sf: 37-51. doi: 10.5194/esd-2-37-2011. | Arşiv Bağlantısı
- R. Marsland, et al. (2017). Limits Of Predictions In Thermodynamic Systems: A Review. Reports on Progress in Physics, sf: 016601. doi: 10.1088/1361-6633/aa9101. | Arşiv Bağlantısı
- K. Michaelian. (2017). Microscopic Dissipative Structuring And Proliferation At The Origin Of Life. Elsevier BV, sf: e00424. doi: 10.1016/j.heliyon.2017.e00424. | Arşiv Bağlantısı
- J. L. Rinn, et al. (2020). Long Noncoding Rnas: Molecular Modalities To Organismal Functions. Annual Reviews, sf: 283-308. doi: 10.1146/annurev-biochem-062917-012708. | Arşiv Bağlantısı
- I. G. Johnston, et al. (2011). Evolutionary Dynamics In A Simple Model Of Self-Assembly. Physical Review E, sf: 066105. doi: 10.1103/PhysRevE.83.066105. | Arşiv Bağlantısı
- C. Mariscal, et al. (2020). Life And Life Only: A Radical Alternative To Life Definitionism. Synthese, sf: 2975-2989. doi: 10.1007/s11229-018-1852-2. | Arşiv Bağlantısı
- W. Martin, et al. (2008). Hydrothermal Vents And The Origin Of Life. Nature Reviews Microbiology, sf: 805-814. doi: 10.1038/nrmicro1991. | Arşiv Bağlantısı
- C. E. Cleland, et al. (2002). Defining ‘Life’. Origins of life and evolution of the biosphere, sf: 387-393. doi: 10.1023/A:1020503324273. | Arşiv Bağlantısı
- I. Fry. (2011). The Role Of Natural Selection In The Origin Of Life. Origins of Life and Evolution of Biospheres, sf: 3-16. doi: 10.1007/s11084-010-9214-1. | Arşiv Bağlantısı
- C. E.. (2019). Moving Beyond Definitions In The Search For Extraterrestrial Life. Astrobiology, sf: 722-729. doi: 10.1089/ast.2018.1980. | Arşiv Bağlantısı
- S. Sarkar, et al. (2019). Design Of Conditions For Self-Replication. Physical Review E, sf: 022414. doi: 10.1103/PhysRevE.100.022414. | Arşiv Bağlantısı
- F. H. C. Crick. (1968). The Origin Of The Genetic Code. Journal of Molecular Biology, sf: 367-379. doi: 10.1016/0022-2836(68)90392-6. | Arşiv Bağlantısı
Evrim Ağacı'na her ay sadece 1 kahve ısmarlayarak destek olmak ister misiniz?
Şu iki siteden birini kullanarak şimdi destek olabilirsiniz:
kreosus.com/evrimagaci | patreon.com/evrimagaci
Çıktı Bilgisi: Bu sayfa, Evrim Ağacı yazdırma aracı kullanılarak 25/05/2026 22:57:12 tarihinde oluşturulmuştur. Evrim Ağacı'ndaki içeriklerin tamamı, birden fazla editör tarafından, durmaksızın elden geçirilmekte, güncellenmekte ve geliştirilmektedir. Dolayısıyla bu çıktının alındığı tarihten sonra yapılan güncellemeleri görmek ve bu içeriğin en güncel halini okumak için lütfen şu adrese gidiniz: https://evrimagaci.org/s/35
İçerik Kullanım İzinleri: Evrim Ağacı'ndaki yazılı içerikler orijinallerine hiçbir şekilde dokunulmadığı müddetçe izin alınmaksızın paylaşılabilir, kopyalanabilir, yapıştırılabilir, çoğaltılabilir, basılabilir, dağıtılabilir, yayılabilir, alıntılanabilir. Ancak bu içeriklerin hiçbiri izin alınmaksızın değiştirilemez ve değiştirilmiş halleri Evrim Ağacı'na aitmiş gibi sunulamaz. Benzer şekilde, içeriklerin hiçbiri, söz konusu içeriğin açıkça belirtilmiş yazarlarından ve Evrim Ağacı'ndan başkasına aitmiş gibi sunulamaz. Bu sayfa izin alınmaksızın düzenlenemez, Evrim Ağacı logosu, yazar/editör bilgileri ve içeriğin diğer kısımları izin alınmaksızın değiştirilemez veya kaldırılamaz.
/profile/2aacbbe4-281f-4f73-9317-6cfea6fc8bc0.jpeg)
/evrimagaci.org/public/images/misc/feed-support-2.png)
/store/products/46aa02b67bba8ca5c79c18ea8d477cc8.png)

/evrimagaci.org/public/images/logo-50.png)